
| A. | 中子数为8的氮原子:8N | |
| B. | 次氯酸的电子式: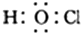 | |
| C. | PCl5分子的每个原子都满足8电子稳定结构 | |
| D. | 用电子式表示NaCl的形成过程: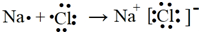 |
分析 A.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
B.次氯酸分子中,Cl原子的最外层满足8电子稳定结构;
C.P的化合价为+5,最外层电子数=5+5=10;
D.氯化钠为离子化合物,阴阳离子需要标出所带电荷,氯离子还需要标出最外层电子.
解答 解:A.中子数为8的氮原子的质量数为15,其正确的表示方法为:715N,故A错误;
B.次氯酸为共价化合物,分子中不存在氢氯键,次氯酸的电子式为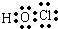 ,故B错误;
,故B错误;
C.PCl5分子中P的最外层电子数=5+5=10,不满足8电子稳定结构,故C错误;
D.NaCl为离子化合物,书写电子式时注意,左边写钠原子和氯原子电子式,右边写氯化钠的电子式,中间用箭头连接,形成过程为: ,故D正确;
,故D正确;
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、核外电子排布、元素符号等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.


科目:高中化学 来源: 题型:选择题
| A. | 温度和体积一定时,容器内压强不再变化 | |
| B. | 生成H2和生成HI的速率相等 | |
| C. | 混合气体的颜色不再变化 | |
| D. | 各物质的物质的量浓度之比为2:1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
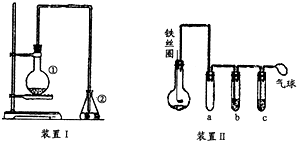 为探究苯与溴的取代反应,甲同学用如图所示的装置Ⅰ进行实验:将一定量的苯和溴放在烧瓶中,同时加入少量铁屑做催化剂,3min后发现滴有AgNO3的锥形瓶中有浅黄色的沉淀生成,即证明苯与溴发生了取代反应.
为探究苯与溴的取代反应,甲同学用如图所示的装置Ⅰ进行实验:将一定量的苯和溴放在烧瓶中,同时加入少量铁屑做催化剂,3min后发现滴有AgNO3的锥形瓶中有浅黄色的沉淀生成,即证明苯与溴发生了取代反应. .
. 与Br2,要想得到纯净的产物,可用NaOH溶液试剂.洗涤后分离粗产吕应使用的仪器是分液漏斗.
与Br2,要想得到纯净的产物,可用NaOH溶液试剂.洗涤后分离粗产吕应使用的仪器是分液漏斗.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
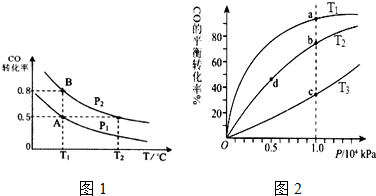
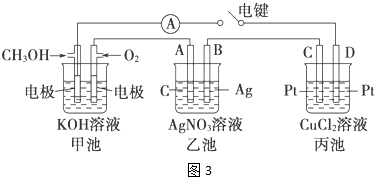
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | N≡N | F-F | N-F |
| 键能:kJ/mol | 941.7 | 154.8 | 283.0 |
| A. | 过程F2(g)→2F(g)吸收能量 | |
| B. | 过程N(g)+3F(g)→NF3(g)放出能量 | |
| C. | 反应N2(g)+3F2(g)=2NF3(g)的△H<0 | |
| D. | NF3吸收能量后如果没有化学键的断裂与生成,仍可能发生化学反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
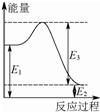 甲烷、一氧化碳和氢气、甲醇等既是重要的燃料也是重要的化工原料.
甲烷、一氧化碳和氢气、甲醇等既是重要的燃料也是重要的化工原料.| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能 (kJ/mol) | 348 | 413 | 436 | 358 | 1072 | 463 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | A-A | B=B | A-B |
| 键能kJ/mol | 236 | 406 | 163 |
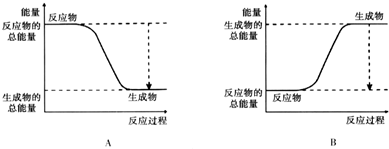
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com