
 .
. .
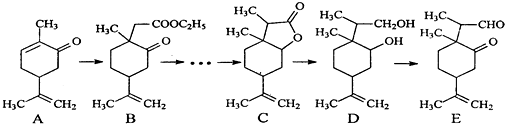
.分析 (1)由B的结构结构简式,可知含氧官能团为酯基、羰基;
(2)反应A→B中需要加入试剂X,其分子式为C4H8O2,属于加成反应,则X为CH3COOC2H5;
(3)避免碳碳双键被H2加成或还原,酯很难和H2发生还原反应;
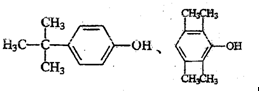
(4)①属于芳香族化合物,说明含有苯环;②能使FeCl3溶液显色,说明含有酚羟基;③核磁共振氢谱显示有4种不同化学环境的氢,结构应对称;
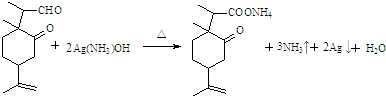
(5)E中醛基与银氨溶液发生氧化反应;
(6)比较B与C的结构简式,可知,B先在氢氧化钠的水溶液中发生水解反应,生成羧酸钠,然后将羰基用LiBH4还原为醇,然后酸化,将羧酸钠变为羧基,羧基与羟基在浓硫酸、加热条件下发生取代反应,生成酯基,最后再与CH3I发生增加C原子的反应得到C.
解答 解:(1)根据B的结构简式可知B中的含氧官能团为羰基和酯基,
故答案为:酯基、羰基;
(2)根据A与B的结构简式的异同,结合X的分子式可知,A转化为B属于加成反应,则X是CH3COOC2H5,
故答案为:CH3COOC2H5;
(3)C→D不直接用H2(镍作催化剂)还原的原因是:因为C中含有碳碳双键,碳碳双键也能与氢气发生加成反应,酯很难和H2发生还原反应,
故答案为:碳碳双键也能与氢气发生加成反应,酯很难和H2发生还原反应;
(4)A的同分异构体满足:①属于芳香族化合物,说明含有苯环;②能使FeCl3溶液显色,说明含有酚羟基;③核磁共振氢谱显示有4种不同化学环境的氢,A的分子式是C10H14O,则分子中存在对称结构,所以符合题意的A的同分异构体的结构简式是 ,
,
故答案为: ;
;
(5)E分子中的醛基可与银氨溶液反应,醛基被氧化为羧基,同时生成氨气、银单质、水,化学方程式是 ,
,
故答案为: ;
;
(6)比较B与C的结构简式,可知,B先在氢氧化钠的水溶液中发生水解反应,生成羧酸钠,然后将羰基用LiBH4还原为醇,然后酸化,将羧酸钠变为羧基,羧基与羟基在浓硫酸、加热条件下发生取代反应,生成酯基,最后再与CH3I发生增加C原子的反应得到C,合成流程图是: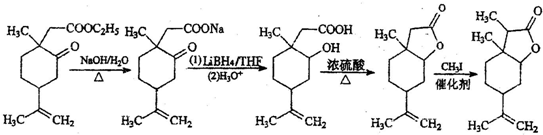 ,
,
故答案为: .
.
点评 本题考查有机物的推断与合成、官能团的判断、同分异构体的书写、化学方程式的书写等,(6)中注意根据转化中隐含的信息进行设计,侧重于学生分析解决问题能力与知识迁移运用的考查.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 原子半径:A<B<C<D<E | |
| B. | 化合物AE与CE含有相同类型的化学键 | |
| C. | 金属性:D>C | |
| D. | D单质能够溶解于C的最高价氧化物对应的水化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常见单质的沸点:W>Y>Z | |
| B. | W的氢化物为共价化合物 | |
| C. | 原子半径:Y<Z<W | |
| D. | X、Y可以形成既有极性键也有非极性键的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
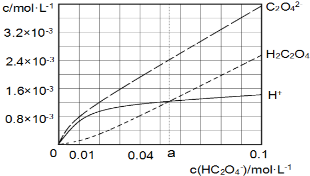 25℃时,往水中不断加入NaHC2O4固体,部分微粒浓度随c(HC2O4)的变化趋势如下图所示.下列说法正确的是( )
25℃时,往水中不断加入NaHC2O4固体,部分微粒浓度随c(HC2O4)的变化趋势如下图所示.下列说法正确的是( )| A. | 当c(HC2O4ˉ)=0.1mol•Lˉ1时,c(H+)>c(C2O42-)-c(H2C2O4) | |
| B. | 当c(HC2O4ˉ)>amol•Lˉ1时,c(H+)<c(H2C2O4),HC2O4ˉ的水解程度大于电离程度 | |
| C. | HC2O4ˉ?C2O42-+H+,Ka(HC2O4ˉ)=a | |
| D. | 将0.08mol•Lˉ1H2C2O4溶液与等浓度NaOH溶液等体积混合后(忽略体积变化),c(Na+)>c(HC2O4ˉ)>c(C2O42-)>c(H2C2O4)>c(H+)>c(OHˉ) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有如下化学反应:2A(g)+B(g)?2C(g),△H<0.
有如下化学反应:2A(g)+B(g)?2C(g),△H<0.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 气化反应式 | 1gK | ||
| 700K | 900K | 1200K | |
| C(s)+H2O(g)=CO(g)+H2(g) | -2.64 | -0.39 | 1.58 |
| C(s)+2H2O(g)=CO2(g)+2H2(g) | -1.67 | -0.03 | 1.44 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔点:Na>MgO>SiO2 | B. | 水溶性:SO2>H2S>HCl | ||
| C. | 热稳定性:HF>H2O>NH3 | D. | 沸点:HF>HCl>HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CH3)2CHCl | B. | CH3C(CH3)2I | C. | (CH3)3COOCCH2CH3 | D. | CH3C(CH3)2CH2Br |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com