
【题目】测得某溶液中含Cu2+ , K+ , SO42﹣ , Cl﹣四种离子且阳离子的个数比为:N(Cu2+):N(K+)=3:4,则SO42﹣与Cl﹣的物质的量之比可能是( )
A.3:2
B.1:3
C.1:8
D.2:5
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
【题目】可用于分离或提纯物质的方法有:过滤、蒸发结晶、蒸馏、萃取、分液、洗气。根据需求填下列装置的序号并填上操作名称:
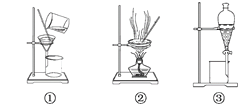
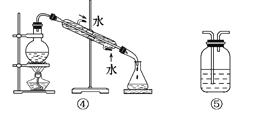
(1)分离Na2CO3溶液和CCl4,选_____,操作名称为________。
(2)用CCl4提取碘水中的碘,选______,操作名称为________。
(3)用氢氧化钠溶液吸收O2中混有的杂质Cl2,选_______,操作名称为________。
(4)除去澄清石灰水中悬浮的CaCO3颗粒选______,操作名称为__________。
(5)制取蒸馏水,选________,操作名称为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取100 mL0.3mol/L和300 mL0.25mol/L的硫酸注入500 mL的容量瓶中,加水稀释至刻度线,则该混合液中H+的物质的量浓度为
A. 0.21mol/L B. 0.26mol/L C. 0.42mol/L D. 0.56mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)2011年,内蒙古、新疆、浙江等地都要陆续召开各具特色的农博会,到时“生态农业”将成为农会人员关注的热门话题。生态农业涉及农家肥料的综合利用,某种肥料经发酵得到一种含甲烷、二氧化碳、氮气的混合气体。2.016 L(标准状况)该气体通过盛有红热CuO粉末的硬质玻璃管,发生的反应为:CH4+4CuO![]() CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8 g。将反应后产生的气体通入过量的澄清石灰水中,充分吸收,生成沉淀8.5 g。
CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8 g。将反应后产生的气体通入过量的澄清石灰水中,充分吸收,生成沉淀8.5 g。
(1)原混合气体中甲烷的物质的量是________。
(2)原混合气体中氮气的体积分数为________。
(二)FeS与一定浓度的HNO3反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO和H2O,当NO2、N2O4、、NO的物质的量之比为1﹕1﹕1时,实际参加反应的FeS与HNO3的物质的量之比为___________________
(三)某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
已知0.2 mol KBrO3在反应中得到1 mol电子生成X,请将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目。_________________
![]() +
+![]()
(四) 在一定条件下,分别以高锰酸钾、氯酸钾、过氧化氢(H2O2)、过氧化钠为原料制取氧气,当制得同温、同压下相同体积的O2时,四个反应中转移的电子数之比为_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子的空间构型可用sp2杂化轨道来解释的是( )
①BF3 ②CH2=CH2 ③![]() ④CH≡CH ⑤NH3 ⑥CH4
④CH≡CH ⑤NH3 ⑥CH4
A. ①②③ B. ①⑤⑥ C. ②③④ D. ③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)从氯化钠溶液中得到氯化钠固体,选择装置____(填代表装置图的字母,下同);除去自来水中的Cl﹣等杂质,选择装置____;从碘水中提取I2,选择装置____,该分离方法的名称为________。
(2)装置A中①的名称是____________,冷却水的方向是______________,温度计水银球的位置是在_____________;装置B在分液时装置中的液体不能顺利滴下,原因是___________________________。
(3)从碘水中提取碘时,不能选用的试剂是______。
A.酒精 B.苯 C.四氯化碳
若选择试剂X(密度小于水的密度)从碘水中提取碘时,充分振荡、静置后,下层液体的颜色为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
B元素原子的核外p电子数比s电子数少1 |
C原子的第一至第四电离能分别是 I1=738 kJ/mol;I2=1 451 kJ/mol;I3=7 733 kJ/mol;I4=10 540 kJ/mol |
D原子核外所有p轨道全满或半满 |
E元素的主族序数与周期数的差为4 |
F是前四周期中电负性最小的元素 |
G在周期表的第七列 |
(1)已知BA5为离子化合物,写出其电子式______________________________。
(2)B基态原子中能量最高的电子,其电子云在空间有________个方向,原子轨道呈________形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布为![]() 该同学所画的电子排布图违背了_____________________________________。
该同学所画的电子排布图违背了_____________________________________。
(4)G位于________族________区,价电子排布式为________。
(5)检验F元素的方法是________,请用原子结构的知识解释产生此现象的原因是_____________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com