
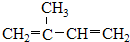 ⑤ClCH=CHCl ⑥
⑤ClCH=CHCl ⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨
 .
.
分析 I、(1)⑧为烷烃,根据烷烃的命名原则对该有机物进行命名,选取最长的链为主链;
(2)同系物是结构相似,在组成上相差CH2原子团的物质互称同系物;同分异构体是分子式相同结构不同的物质;根据具有顺反异构体的有机物中C=C应连接不同的原子或原子团;
(3)甲苯苯环上的一氯取代物可以看作甲苯中1个氢原子被1个氯原子取代,甲苯苯环上有5个氢原子,环上的四氯代物可以看作苯环五氯代物其中1个氯原子被1个氢原子取代,故一氯代物与四氯代物同分异构体数目相同;甲苯在浓硫酸作用下可与浓硝酸反应生成TNT;
II、凡链节主链上只有碳原子并存在碳碳双键结构的高聚物,其规律是“见双键,四个碳,无双键,两个碳”画线断开,然后将半键闭合,即将单双键互换,即可得到单体.
解答 解:(1)⑧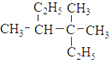 为烷烃,最长碳链含有6个碳,其主链为己烷,在3号C含有2个甲基,在4号C含有1个甲基,其名称为:3,3,4-三甲基己烷;
为烷烃,最长碳链含有6个碳,其主链为己烷,在3号C含有2个甲基,在4号C含有1个甲基,其名称为:3,3,4-三甲基己烷;
故答案为:3,3,4-三甲基己烷;
(2)②3-甲基-1-氯戊烷与⑦ 分子式相同,结构不同,属于同分异构体;
分子式相同,结构不同,属于同分异构体;
①与⑧均为饱和烷烃,结构相似、分子式不同,故属于同系物,③和⑨均含有1个苯环,且分子式不同,互为苯的同系物;
⑤ClCH=CHCl为1,2-二氯乙烯,碳碳双键上的C连接不同原子或原子团,存在顺反异构;
故答案为:②和⑦;①和⑧、③和⑨;⑤;
(3)甲苯有3种不同的H原子,故一氯代物有3种,分别为邻位取代,间位取代和对位取代,甲苯苯环上有5个氢原子,一氯代物与四氯代物同分异构体数目相同,所以苯环上的四氯代物有3种;在浓硫酸作用下可与浓硝酸反应生成TNT,反应的化学方程式为 ;
;
故答案为:3; ;
;
II、根据“凡链节主链上只有碳原子并存在碳碳双键结构的高聚物,其规律是“见双键,四个碳,无双键,两个碳”画线断开,然后将半键闭合,即可得到单体”知,该高分子有机物的单体是:CH2=CH2、CH2=CHCN、CH≡CH;
故答案为:CH2=CH2;CH2=CHCN;CH≡CH.
点评 主要考查了烃、同系物、同分异构体概念的理解,有机物的结构片段判断单体等,难点是根据有机物的结构片段判断单体.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 实验室有一试剂瓶的标签严重破损,只能隐约看到如图所示部分,取该试剂瓶中的试剂,通过燃烧实验测得:0.1mol该物质完全燃烧只得到39.6gCO2和9gH2O.
实验室有一试剂瓶的标签严重破损,只能隐约看到如图所示部分,取该试剂瓶中的试剂,通过燃烧实验测得:0.1mol该物质完全燃烧只得到39.6gCO2和9gH2O.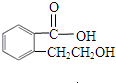 ;
;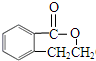 .
.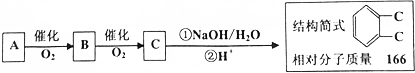
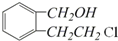 ;
;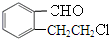 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 ;
;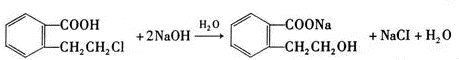 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=+890 kJ/mol | |
| B. | CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890kJ/mol | |
| C. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-445kJ/mol | |
| D. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①④ | B. | ②④ | C. | ②③ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
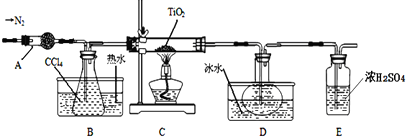
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 化学方程式或结论 |
| 金属Na长时间放置在空气中 | 银白色的金属光泽消失,迅速变暗,有水珠生成,最终生成白色的粉末 | ①4Na+O2═2Na2O Na2O+H2O═2NaOH 2Na+2H2O═2NaOH+H2↑ 2NaOH+CO2═Na2CO3+H2O |
| 将一块Na置于石棉网上,点燃酒精灯加热 | 钠先熔成小球,剧烈燃烧并发出黄色的火焰,生成②淡黄色色的粉末 | 2Na+O2 ═Na2O2 |
| 往上述生成的 Na2O2上滴加蒸馏水 | 生成的气体能使带火星的木条复燃 | 该气体为③O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com