
| A、用H2表示的反应速率为0.1 mol?L-1?min-1 |
| B、用N2表示的反应速率为0.04 mol?L-1?s-1 |
| C、用N2表示的反应速率为0.2 mol?L-1?s-1 |
| D、用NH3表示的反应速率为0.3 mol?L-1?s-1 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
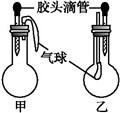 |
甲 | 乙 | |||
| 滴管中 | 烧瓶中 | 滴管中 | 烧瓶中 | ||
| A | 水 | 过氧化钠 | 饱和碳酸氢钠溶液 | CO2 | |
| B | 水 | 钠 | 饱和碳酸钠溶液 | CO2 | |
| C | NaOH溶液 | 碳酸氢钠 | 澄清石灰水 | 碳酸氢钠 | |
| D | 稀盐酸 | 碳酸氢钠 | NaOH溶液 | CO2 | |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2H2(g)+O2(g)=2H2O(l);△H=-285.8 kJ/mol | ||
B、H2(g)+
| ||
C、H2O(l)=H2(g)+
| ||
| D、2H2+O2=2H2O;△H=-571.6 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的 |
| B、酸性氧化物都是非金属氧化物 |
| C、可利用焰色反应鉴别氯化钠和硫酸钾 |
| D、在水溶液中能电离出氢离子的物质为酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,等质量的硫蒸气和硫固体分别在氧气中完全燃烧,前者放出热量比后者少 |
| B、由C(石墨)=C(金刚石)△H=+1.90 kJ/mol可知,金刚石比石墨稳定 |
| C、在稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ/mol,若将含0.5 mol H2SO4的稀硫酸与含0.5mol Ba(OH)2 的氢氧化钡溶液混合,放出的热等于57.3 kJ |
| D、在101 kPa时,2 g H2 完全燃烧生成液态水,放出285.8 kJ热量,则氢气燃烧的热化学方程式可以表示为:2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子得电子能力Y<Z |
| B、该化合物一定为共价化合物 |
| C、该化合物一定为强电解质 |
| D、该化合物的化学式一定为X2YZ4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2、O2、SO3的浓度之比为 2:1:2 |
| B、SO2、O2、SO3的浓度均不再变化 |
| C、单位时间内消耗1molO2同时生成2molSO3 |
| D、SO2、O2、SO3共存 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com