
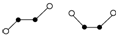
 W��Y��Z��Q��R�����ڱ���ǰ�����ڵ�Ԫ�أ���ԭ��������������̬W��ԭ�Ӻ�����2��δ�ɶԵ��ӣ�Q�ǵ縺������Ԫ�أ���̬R��ԭ�Ӻ���δ�ɶԵ�������Wԭ�Ӻ���δ�ɶԵ�������2�������ʴ��������⣨����ʱ��W��Y��Z��Q��R������Ӧ��Ԫ�ط��ű�ʾ����
W��Y��Z��Q��R�����ڱ���ǰ�����ڵ�Ԫ�أ���ԭ��������������̬W��ԭ�Ӻ�����2��δ�ɶԵ��ӣ�Q�ǵ縺������Ԫ�أ���̬R��ԭ�Ӻ���δ�ɶԵ�������Wԭ�Ӻ���δ�ɶԵ�������2�������ʴ��������⣨����ʱ��W��Y��Z��Q��R������Ӧ��Ԫ�ط��ű�ʾ����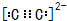 ����̬Rԭ�ӵļ۵����Ų�ʽΪ3d64s2��
����̬Rԭ�ӵļ۵����Ų�ʽΪ3d64s2������ W��Y��Z��Q��R�����ڱ���ǰ�����ڵ�Ԫ�أ���ԭ��������������Q�ǵ縺������Ԫ�أ���QΪFԪ�أ�Wԭ�Ӻ�����2��δ�ɶԵ��ӣ�ԭ������С��F���������Ϊ3�����ڵڶ����ڣ�W��������Ų�Ϊ1s22s22p2����WΪCԪ�أ����ԭ��������֪��YΪNԪ�ء�ZΪOԪ�أ�RԪ�ص�ԭ�Ӻ����δ�ɶԵ�������Wԭ�Ӻ���δ�ɶԵ�������2������Rԭ��δ�ɶԵ�����Ϊ4����R���ڵ������ڣ���ԭ�Ӻ�������Ų�Ϊ1s22s22p63s23p63d64s2����RΪFeԪ�أ��Դ˽����⣮
��� �⣺��1��ͬ�����������Ԫ�ص�һ�����ܳ��������ƣ���NԪ�ص�2p�ܼ�����3�����ӣ����ڰ����ȶ�״̬�������ϵͣ���һ�����ܸ���ͬ��������Ԫ�أ��ʵ�һ������N��O��C������������Ԫ�ص�ԭ���У���CO2��Ϊ�ȵ�����ķ���ʽN2O��
�ʴ�Ϊ��N��O��C�� N2O��
��2��Fԭ�ӳ�һ�����ۼ�����ģ�Ϳ�֪����ɫ���ʾF����ɫ���ʾN��Nԭ��֮��Ӧ��N=N˫����N2F2������Nԭ�Ӽ۲���Ӷ���=2+$\frac{5-1-2}{2}$=3��Nԭ�Ӳ�ȡsp2�ӻ���
�ʴ�Ϊ��sp2��
��3��C22-��������Cԭ��֮���γ����Թ��õ��Ӷԣ��Ҷ�����8�����ȶ��ṹ�������ʽΪ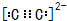 ��RΪFeԪ�أ�ԭ�Ӻ���۲�����Ų�Ϊ3d64s2��
��RΪFeԪ�أ�ԭ�Ӻ���۲�����Ų�Ϊ3d64s2��
�ʴ�Ϊ��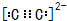 ��3d64s2��
��3d64s2��
��4��NF3������Nԭ�Ӽ۲���Ӷ���=3+$\frac{5-1��3}{2}$=4��Nԭ�Ӻ���1�Թ¶Ե��ӣ�����ռ乹��Ϊ�����Σ�
Y��Q��Ԫ�ص��⻯��ֱ�ΪNH3��HF�����ڵ縺��F��N����HF����֮��������NH3����֮��������ǿ����HF�ķ��»�����ǿ����HF�ķе���ߣ�
���ڵ縺��F��N��H��NF3�����й��õ��Ӷ�ƫ��Fԭ�ӣ�ʹ��Nԭ���ϵŶԵ�������Cu2+�γ�����
�ʴ�Ϊ�������Σ�HF�����ڵ縺��F��N��H��NF3�����й��õ��Ӷ�ƫ��Fԭ�ӣ�ʹ��Nԭ���ϵŶԵ�������Cu2+�γ�����
��5����ѧ��ͨ��X����̽��FeO�ľ���ṹ��NaCl����ṹ���ƣ�����ΪFe2+���ģ���FeO�����о���Fe2+����ҵȾ����Fe2+λ����������ϣ��ʹ���12����FeO�ľ���ṹ��NaCl�ľ���ṹ���ƣ���һ�������к���4����FeO����NA����FeO��������Ϊ72g��FeO�������������Ӽ��������Ϊa��10-10 cm�������Ϊ��2a cm��3=8a3��10-30 cm3����������Ϊ8a3 ��10-30 cm3����g/cm3=8��a3��10-30 g������$\frac{72g}{{N}_{A}}$��4=8��a3��10-30 g����NA=$\frac{36}{��{a}^{3}}$��1030 ���ʴ�Ϊ��12��$\frac{36}{��{a}^{3}}$��1030 ��
���� ���⿼�����ʽṹ�����ʣ�Ϊ��Ƶ���㣬�漰��������Ų����ɡ������ܡ����ӽṹ���ӻ��������������������ṹ�����ȣ��ѶȽϴ�5��Ϊ�״��㡢�ѵ㣬��Ҫѧ��ʶ�dz�������ľ����ṹ��


 ϰ�⾫ѡϵ�д�
ϰ�⾫ѡϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
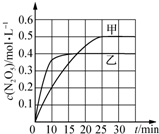 �������������������������������ӦΪ��2NO2��g��+O3��g��?N2O5��g��ʮO2��g����H����ͬ�¶��£������������з���������Ӧ�������Ϣ�����ͼ��ʾ��
�������������������������������ӦΪ��2NO2��g��+O3��g��?N2O5��g��ʮO2��g����H����ͬ�¶��£������������з���������Ӧ�������Ϣ�����ͼ��ʾ��| ���� | �� | �� | �� |
| �ݻ�/L | 1 | 1 | 2 |
| ��Ӧ�� | |||
| ��ʼ�� | 2mol NO2 | ||
| 1mol O3 | 2mol NO2 | ||
| 1mol O3 | 2mol N2O5 | ||
| 1mol O2 | |||
| �¶�/K | T1 | T2 | T2 |
| A�� | 0��10 min�ڼ������з�Ӧ��ƽ�����ʣ�v��NO2��=0.02 mol•L-1•min-1 | |
| B�� | T1��T2����H��0 | |
| C�� | ƽ��ʱN2O5Ũ�ȣ�c����N2O5����c����N2O5�� | |
| D�� | T1Kʱ������ʼʱ���������г���2 mol NO2��1 mol O3��2 mol N2O5��2 mol O2����������Ӧ�ﵽƽ��ǰ��v��������v���棩 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
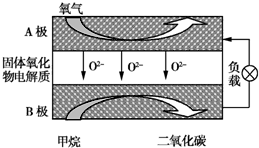 2013��12��17�գ��й�������Դ���ٿ����ŷ����ᣬ�����ڹ㶫�غ��齭����ض��������״����ߴ��ȿ�ȼ������ȼ������Ҫ�ɷ��Ǽ��飬�����������ȼ�ϣ�Ҳ����Ҫ�Ļ���ԭ�ϣ�
2013��12��17�գ��й�������Դ���ٿ����ŷ����ᣬ�����ڹ㶫�غ��齭����ض��������״����ߴ��ȿ�ȼ������ȼ������Ҫ�ɷ��Ǽ��飬�����������ȼ�ϣ�Ҳ����Ҫ�Ļ���ԭ�ϣ�| ���� | H2 | CO | CH3OH |
| Ũ��/��mol•L-1�� | 0.20 | 0.10 | 0.40 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
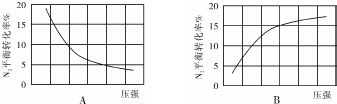
| ��� | �¶� | N2��ʼ��/mol | N2�����ʵ���/mol | ||||||
| 5��s�� | 10��s�� | 15��s�� | 20��s�� | 25��s�� | 30��s�� | 35��s�� | |||
| �� | T1 | 0.1 | 0.094 | 0.089 | 0.085 | 0.0825 | 0.081 | 0.080 | 0.080 |
| �� | T2 | 0.1 | 0.090 | 0.085 | 0.082 | 0.080 | 0.080 | 0.080 | 0.080 |
| �� | T3 | 0.2 | 0.179 | 0.165 | 0.153 | 0.146 | x | x | x |
| �� | T4 | 0.2 | 0.173 | 0.161 | 0.155 | 0.150 | 0.150 | 0.150 | 0.150 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | Zn��s��+CuSO4��aq��=ZnSO4��aq��+Cu��s������H=-216kJ•mol-1����Ӧ��������С�������������� | |
| B�� | ��ͬ�����£����1 mol��ԭ�������е�����ΪE1��1mol����ӵ�����ΪE2����2E1��E2 | |
| C�� | 101kPaʱ��2H2��g��+O2��g��=2H2O��1������H=-571.6kJ•mol-1����������̬ˮ����HС��-571.6kJ•mol-1 | |
| D�� | ����̫���ܵ������Դ���滯ʯȼ�ϣ������ڽ�Լ��Դ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| A | B | C | |
| D | E | F |
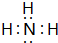 ��ʵ������ȡ����Ļ�ѧ����ʽΪ2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��
��ʵ������ȡ����Ļ�ѧ����ʽΪ2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��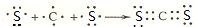 ��
��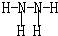 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�22.4LH2O���еķ�����ΪNA | |
| B�� | ���³�ѹ�£�32g O2���е���ԭ����Ϊ2NA | |
| C�� | ͨ��״���£�NA��CO2����ռ�е����Ϊ22.4L | |
| D�� | 1L 0.1mol/L NaCl��Һ��������Na+ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
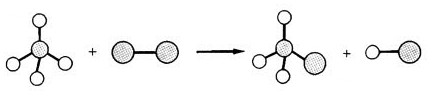
| A�� | ȡ����Ӧ | B�� | �ӳɷ�Ӧ | C�� | �ۺϷ�Ӧ | D�� | ������Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com