
| 压强/MPa 体积分数/% 温度/℃ | 2.0 | 4.0 | 6.0 |
| 700 | 55.0 | a | b |
| 850 | c | 75.0 | d |
| 950 | e | f | 85.0 |
分析 反应A(g)+B(s)?2C(g)中B为固体,生成物气体的计量数大于反应物气体的计量数,则增大压强,平衡逆向移动,则a<55.0,由表中数据可知升高温度,C的体积分数增大,说明平衡正向移动,则正反应为吸热反应,850℃、4.0MPa时C的体积分数为75%,可结合三段式法计算.
解答 解:(1)反应A(g)+B(s)?2C(g)中B为固体,生成物气体的计量数大于反应物气体的计量数,则增大压强,平衡逆向移动,则a<55.0,第3列数据中75.0>a,说明升高温度平衡向正反应方向移动,正反应为吸热反应,则△H>0,故答案为:>;
(2)增大压强,平衡逆向移动,C的体积分数减小,则a>b,正反应为吸热反应,升高温度平衡正向移动,则e>f>a>b,故答案为:e>f>a>b;
(3)正反应为吸热反应,升高温度平衡正向移动,则平衡常数增大,K(700℃)<K(950℃),故答案为:<;
(4)850℃、4.0MPa时C的体积分数为75%,设A为1mol,转化xmol,则
A(g)+B(s)?2C(g)
起始 1mol 0
转化 xmol 2xmol
平衡(1-x)mol 2xmol
$\frac{2x}{1-x+2x}$=75%,
x=0.6,
则850℃、4.0MPa时A的转化率为$\frac{0.6}{1}×100%$=60%.
故答案为:60%.
点评 本题考查化学平衡计算、平衡移动等,为高频考点,旨在考查学生对数据的分析能力、计算能力,注意把握反应方程式的特点以及温度、压强对平衡移动的影响,难度中等.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:选择题
| A. | 无色透明的溶液中:Cu2+、K+、SO42-、NO3- | |
| B. | 使无色酚酞试液呈红色的溶液中:Na+、K+、SO42-、CO32- | |
| C. | NH4Cl溶液中:K+、OH-、SO42-、Cl- | |
| D. | pH=1的溶液中:Na+、K+、HCO3-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
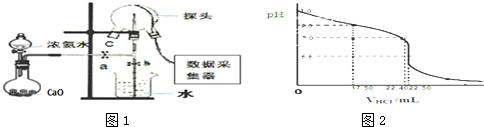
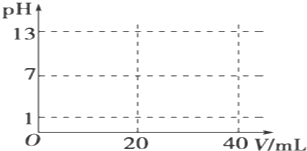
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 滴定前读数(mL) | 滴定后读数(mL) |
| 1 | 0.00 | 20.10 |
| 2 | 1.00 | 20.90 |
| 3 | 0.00 | 21.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
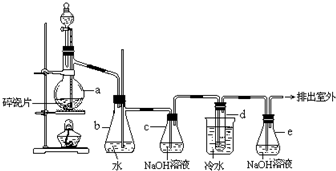
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
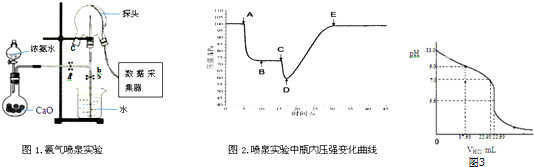
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表:
实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表:| 化合物 | 相对分 子质量 | 密度 /(g•cm-3) | 沸点/℃ | 溶解度 /(g/100g水) |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上用石灰乳制备漂白粉:Ca(OH)2+Cl2=Ca2++ClO-+Cl-+H2O | |
| B. | 向硫酸铝铵溶液中滴加少量Ba(OH)2溶液:NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3•H2O+2H2O | |
| C. | 制备Fe(OH)3胶体:Fe3++3H2O?Fe(OH)3(胶体)+3H+ | |
| D. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com