
| A. | 只有①②③ | B. | 只有①②④ | C. | 只有①③④ | D. | ①②③④ |
分析 ①结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物.同系物具有如下特点:结构相似、化学性质相似、分子式通式相同,分子式不同、物理性质不同,研究范围是有机物;
②结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物;
③烃中碳、氢元素的质量分数相同,则最简式相同;
④具有同一通式的物质不一定属于同系物.
解答 解:①同系物结构相似,化学性质相似,但化学性质相似物质不一定是同系物,如乙醇与甘油,故①错误;
②同系物在分子组成上析出相差一个或若干个CH2原子团,但相差一个或若干个CH2原子团的有机物不一定是同系物,如乙酸与乙酸乙酯,故②错误;
③烃中碳、氢元素的质量分数相同,则只能说明最简式相同,而同系物中碳、氢元素的质量分数不一定对应相同,如甲烷与乙烷.烃中碳、氢元素的质量分数对应相同,不一定是同系物如乙炔与苯,故③错误;
④具有同一通式的物质不一定属于同系物,故乙烯和环丙烷均符合CnH2n的通式,但不是同系物,故④错误.
故选D.
点评 考查同系物的概念,难度较小,注意有机“五同”概念的辨析与理解.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 原子半径大小顺序:W>Z>Y>X | |
| B. | Z在周期表中的位置是第三周期第IA族 | |
| C. | X的气态氢化物的还原性比W的弱 | |
| D. | W比Y更容易与氢气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH-CH=CH2 1,3-二丁烯 | B. | 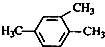 1,3,4-三甲苯 1,3,4-三甲苯 | ||
| C. | CH3CH2CH(OH)CH3 2-丁醇 | D. | 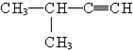 2-甲基-3-丁炔 2-甲基-3-丁炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
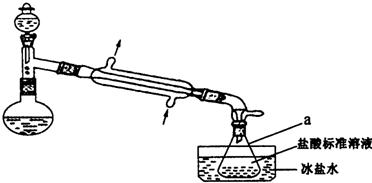 某实验小组以CoCl2•6H2O、过氧化氢、液氨、氯化铵固体为原料,在活性炭催化下,合成了橙黄色晶体X.为确定其组成,他们进行了如下实验:
某实验小组以CoCl2•6H2O、过氧化氢、液氨、氯化铵固体为原料,在活性炭催化下,合成了橙黄色晶体X.为确定其组成,他们进行了如下实验:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素Y的最高正化合价+6 | |
| B. | 简单离子半径的大小顺序为W>Q>Z>X>Y | |
| C. | 气态氢化物的稳定性:Q>W | |
| D. | 元素W的最高价氧化物对应的水化物酸性比Q的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水 | B. | NaNO3溶液 | C. | NaCl溶液 | D. | CuSO4粉末 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | I2O5 | B. | I2O4 | C. | I4O5 | D. | I4O9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com