
| A、混合气体中一定有甲烷 |
| B、混合气体中一定是甲烷和乙烯 |
| C、混合气体中一定有乙烷 |
| D、混合气体中一定有乙炔(CH≡CH) |
| 3.6g |
| 18g/mol |
| 3.6g |
| 18g/mol |


科目:高中化学 来源: 题型:
| A、石墨烯属于共价化合物 |
| B、该材料吸油过程为物理变化 |
| C、碳纳米管和石墨烯互为同位素 |
| D、碳纳米属于胶体分散系 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
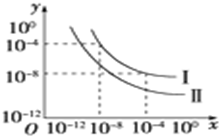 在不同温度下的水溶液中c(H+)=10x mol/L,c(OH-)=10y mol/L,x与y的关系如图所示.请回答下列问题:
在不同温度下的水溶液中c(H+)=10x mol/L,c(OH-)=10y mol/L,x与y的关系如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酒精消毒是对蛋白的变性作用 |
| B、天然皮革是变性蛋白质 |
| C、误食重金属盐会使人中毒,可以服用鸡蛋清帮助解毒 |
| D、坏血病患者应该多吃的食物是鱼肉和猪肉 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中.“硫酸法”生产钛的原料是钛铁矿(主要成分是:FeTiO3,还含有少量Mn、Zn、Cr、Cu等重金属元素及脉石等杂质);主要生产流程如下:
金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中.“硫酸法”生产钛的原料是钛铁矿(主要成分是:FeTiO3,还含有少量Mn、Zn、Cr、Cu等重金属元素及脉石等杂质);主要生产流程如下:
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com