
科目:高中化学 来源:2015-2016学年江西省高一下学期期中考试化学试卷(解析版) 题型:选择题
根据热化学方程式:S(l)+O2(g) SO2(g)△H= -293.23kJ/mol,分析下列说法正确的是( )
SO2(g)△H= -293.23kJ/mol,分析下列说法正确的是( )
A、S(s)+O2(g) SO2(g),反应放出的热量大于293.23kJ/mol
SO2(g),反应放出的热量大于293.23kJ/mol
B、S(s)+O2(g) SO2(g),反应放出的热量小于293.23kJ/mol
SO2(g),反应放出的热量小于293.23kJ/mol
C、1molSO2(g)的化学键断裂吸收的能量总和大于1molS(l)和1molO2(g)的化学键断裂吸收的能量之和。
D、1molSO2(g)的化学键断裂吸收的能量总和小于1molS(l)和1molO2(g)的化学键断裂吸收的能量之和。
查看答案和解析>>
科目:高中化学 来源:2016届辽宁师大附中高三下学期精品考试理综化学试卷(解析版) 题型:填空题
氨对人类的生产生活具有重要影响。
(1)氨的制备与利用。
① 工业合成氨的化学方程式是 。
② 氨催化氧化生成一氧化氮反应的化学方程式是 。
(2)氨的定量检测。
水体中氨气和铵根离子(统称氨氮)总量的检测备受关注。利用氨气传感器检测水体中氨氮含量的示意图如下:
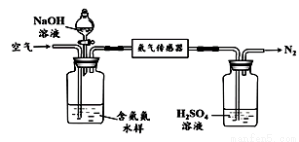
① 利用平衡原理分析含氨氮水样中加入NaOH溶液的作用: 。
② 若利用氨气传感器将1 L水样中的氨氮完全转化为N2时,转移电子的物质的量为6×10-4 mol ,则水样中氨氮(以氨气计)含量为 mg·L-1。
(3)氨的转化与去除。
微生物燃料电池(MFC)是一种现代化氨氮去除技术。下图为MFC碳氮联合同时去除的氮转化系统原理示意图。
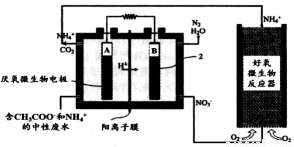
① 已知A、B两极生成CO2和N2,写出A极的电极反应式: 。
② 用化学用语简述NH4+去除的原理: 。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三考前热身(五模)化学试卷(解析版) 题型:选择题
常温下,用0.1mol•L-1HCl溶液滴定10.0mL浓度为0.1mol•L-1Na2CO3溶液,所得滴定曲线如图所示。下列微粒浓度大小关系正确的是
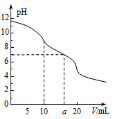
A.当V=0时:c(H+)+c(HCO3-)+2c(H2CO3)=c(OH-)
B.当V=5时:c(CO32-)+c(HCO3-)+c(H2CO3)=2c(Cl-)
C.当V=10时:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
D.当V=a时:c(Na+)=c(Cl-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三考前热身(五模)化学试卷(解析版) 题型:选择题
用下列装置进行相应实验,能达到实验目的的是
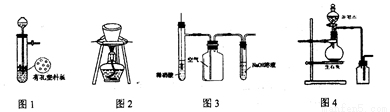
A. 图1所示装置用于Cu和浓硫酸反应制取少量的SO2气体
B. 图2装置用于除去碳酸氢钠固体中的少量碳酸钠
C. 图3装置用于制备并收集NO气体
D. 图4所示装置制取并收集氨气
查看答案和解析>>
科目:高中化学 来源:2016届海南师大附中高三临考模拟化学试卷(解析版) 题型:选择题
碳、硫、氧、氮是中学常见元素,下列说法正确的是( )
A.CO2、SO2、NH 3都是直线形分子
B.CO2、NH3、H2S 的键角依次减小
C.H2O2、N2H4分子的中心原子都是sp3杂化
D.C、N、F元素的电负性依次减小
查看答案和解析>>
科目:高中化学 来源:2016届海南师大附中高三临考模拟化学试卷(解析版) 题型:填空题
A、B、C、D均为短周期元素,他们的原子序数依次增大,B是构成物质种类最多的元素,B和A组成的化合物 B6 A 6 是一种无色透明的液体,不溶于水,密度比水小,C 是地壳中含量最高的非金属元素,D 在同周期元素中原子半径最大。
(1)A、B、D 的元素名称分别为___________、____________、___________
(2)C 在元素周期表中位置为___________________。
(3)A、C、D 能组成多种不同的化合物,这些化合物中既含有极性共价键又含有离子键的化合物为_______________(写电子式,下同),既含有非极性共价键又含有离子键的化合物为_________________。
(4)A 和 D 能组成一种化学活性很高的离子化合物 DA,DA 能和C的单质 C2反应生成一种强碱,请写出 DA 和 C2反应的化学方程式_________________________。
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三下冲刺模拟理综化学C卷(解析版) 题型:实验题
工业上可以用汞阴极法电解NaCl溶液得到烧碱与氯气、氢气,装置见下图:
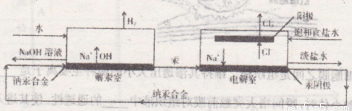
利用烧碱与氯气还可生产一种高效的多功能的水处理剂高铁酸钾。主要的生产流程如下:
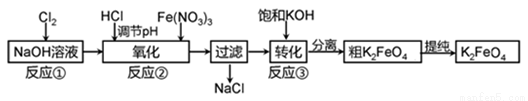
(1)写出汞阴极法的阴极电极反应式_____________;解汞室内的反应化学方程式____________。
(2)反应原理如下:
反应①:Cl2+2NaOH=NaCl+NaClO+H2O
氧化过程化学方程式:______________________;
若加入过量NaClO,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式__________________;
转化过程:Na2FeO4+2KOH=K2FeO4+2NaOH,该过程在某低温下进行的,说明些温度下Ksp(K2FeO4)_____Ksp(Na2FeO4)(填“>”、“<”、“=”)。
(3)实验室在过滤时用到的玻璃仪器有______________________;
(4)既能起到杀菌作用又能起到净水作用,原因是其在水溶液中易水解产生氧气,请写出其水解化学方程式_____________________;
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁沈阳二中高一6月月考化学试卷(解析版) 题型:选择题
将固体NH4I置于密闭容器中,在一定温度下发生下列反应:①NH4I(s) NH3(g)+HI(g) ②2HI(g)
NH3(g)+HI(g) ②2HI(g) H2(g)+I2(g) 达到平衡时,c(H2)=1.0 mol·L-1,c(HI)=4mol·L-1,则此温度下反应①的平衡常数为
H2(g)+I2(g) 达到平衡时,c(H2)=1.0 mol·L-1,c(HI)=4mol·L-1,则此温度下反应①的平衡常数为
A.16 B.20 C.24 D.36
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com