
| A. | △H>0,△S>0 的反应任何条件都是非自发反应 | |
| B. | 放热反应均能自发进行,且反应放出的热量越多,反应越完全 | |
| C. | 某反应的△H>0、△S<0,则该反应一定不能正向进行 | |
| D. | 水从固态→液态→气态的变化过程中△S>0 |
分析 A、根据自发进行的条件是△H-T△S<0分析判断;
B、反应自发与否决定于焓变和熵变两个因素;
C、根据自发进行的条件是△H-T△S<0分析判断;
D、固态→液态→气态,混乱度增大.
解答 解:A、自发进行的条件是△H-T△S<0分析判断,△H>0,△S>0,高温下反应可以自发进行,故A错误;
B、放热的熵减小的反应高温下不能自发进行,故B错误;
C、△H>0、△S<0的反应,△H-T•△S>0,该反应一定不能自发进行,但在一定条件下可以正向进行,如:电解饱和食盐水,在通电的条件下可以正向进行,但是不能自发进行,故C错误;
D、水由固态→液态→气态,混乱度增大,△S>0,故D正确;
故选D.
点评 本题考查反应热与焓变,难度不大,注意反应能否自发进行取决于焓变和熵变的综合判据,不能把其中一个因素当做判断反应能自发进行的依据,学习中注意该部分知识的积累.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO+H2O?CO2+H2 | B. | H2PO4-+H2O?HPO42-+H3O+ | ||
| C. | Cl-+H2O?HCl+OH- | D. | HS-+H2O?H2S+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2S通入CuSO4溶液中 S2-+Cu2+=CuS↓ | |
| B. | AgCl投入KI溶液中 Ag++I-=AgI↓ | |
| C. | Na2S的水解反应 S2-+2H2O?H2S+2OH- | |
| D. | NH4NO3溶液呈酸性 NH4++H2O?NH3•H2O+H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
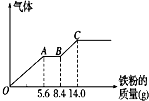 向 100mL 某稀硫酸和稀硝酸的混合溶液中逐渐加入铁粉,产生气体的量(相同状况)随铁粉 质量增加的变化如图所示(已知硝酸只被还原为 NO 气体).下列分析或结果错误的是( )
向 100mL 某稀硫酸和稀硝酸的混合溶液中逐渐加入铁粉,产生气体的量(相同状况)随铁粉 质量增加的变化如图所示(已知硝酸只被还原为 NO 气体).下列分析或结果错误的是( )| A. | OA 段产生的是 NO,BC 段产生氢气,溶液中最终溶质为 FeSO4 | |
| B. | AB 段的反应为 Fe+2Fe3+═3Fe2+, | |
| C. | 原混合酸中NO3-物质的量为 0.3mol | |
| D. | H2SO4 浓度为 2.5 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 滴定前 | 第一次终点 | 第二次终点 | 第三次终点 | |
| 滴定管 液面刻度 | 0.00mL | 16.02mL | 16.00mL | 16.01mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5mol | B. | 1mol | C. | 2mol | D. | 5mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com