
| 选项 | 实验设计 | 实验目的 |
| A | 过氧化钠与水反应 | 制备少量干燥的氧气 |
| B | 取铁在氧气中充分燃烧后的固体产物溶于稀硫酸,加KSCN溶液 | 检验铁的燃烧产物中含+3价铁 |
| C | 分别取大小相近的钠粒、钾粒投入水中,观察反应的剧烈程度 | 比较钠、钾的还原性强弱 |
| D | 将CO2气体通入Na2SiO3溶液中 | 比较C、Si元素非金属性的强弱 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.过氧化钠与水反应生成氧气;
B.铁离子遇KSCN溶液变红色;
C.与水反应生成氢气的剧烈程度越强,金属的金属性越强;
D.最高价氧化物的水化物的酸性越强,则元素的非金属越强.
解答 解:A.过氧化钠与水反应生成氧气,可制取氧气,但不干燥,故A错误;
B.铁离子遇KSCN溶液变红色,可证明燃烧产物中含+3价铁,故B正确;
C.与水反应生成氢气的剧烈程度K>Na,金属性K>Na,故C正确;
D.最高价氧化物的水化物的酸性越强,则元素的非金属越强,所以向饱和Na2SiO3溶液中通入二氧化碳,能比较碳与硅的非金属性强弱,故D正确.
故选A.
点评 本题考查化学实验方案的评价,侧重于学生的分析能力和实验能力的考查,为高考常见题型,注意相关知识的学习与积累,难度不大.


科目:高中化学 来源: 题型:解答题
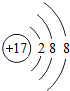 ;
;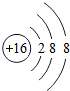 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
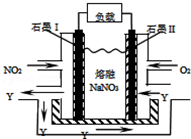 碳和氮的许多化合物在工农业生产和生活中有重要的作用.
碳和氮的许多化合物在工农业生产和生活中有重要的作用.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HA电离出的c(H+)与水电离出的c(H+)之比为108 | |
| B. | 升高温度,溶液的pH减小 | |
| C. | 溶液的pH=4 | |
| D. | HA的电离平衡常数约为l×10-7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁红属于盐类 | B. | 明矾属于碱类 | ||
| C. | SiO2属于酸性氧化物 | D. | NaHCO3属于酸类 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  用石斧解剖 | B. |  早期的农业耕作 | C. |  简单机械织布 | D. |  祥云火炬燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质 | B. | 氧化物 | C. | 无机物 | D. | 有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2(HCl):用饱和NaHCO3溶液 | B. | CO2(SO2):用饱和KMnO4溶液 | ||
| C. | Cl2(HCl):用饱和NaCl溶液 | D. | SO2(HCl):用饱和NaOH溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com