
【题目】25℃时,H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图所示。
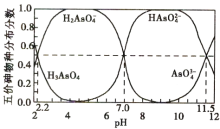
下列叙述错误的是
A.将NaOH溶液逐滴加入到H3AsO4溶液中,当溶液pH在5~6时发生反应的离子方程式为![]()
B.Na2HAsO4溶液中离子浓度关系c(Na+)>c(HAsO![]() )>c(OH-)>c(H2AsO
)>c(OH-)>c(H2AsO![]() )>c(AsO
)>c(AsO![]() )
)
C.向H3AsO4溶液滴加NaOH溶液至中性时c(Na+)=2c(HAsO![]() )+3c(AsO
)+3c(AsO![]() )
)
D.AsO43-第一步水解的平衡常数的数量级为10-3
【答案】C
【解析】
A.当溶液pH在5~6时,H2AsO![]() 的分布分数由1开始降低,HAsO
的分布分数由1开始降低,HAsO![]() 的分布分数由0开始增加,故发生反应
的分布分数由0开始增加,故发生反应![]() ,A正确;
,A正确;
B.当pH=11.5时,c(HAsO![]() )=c(AsO43-),求得
)=c(AsO43-),求得![]() ,则HAsO
,则HAsO![]() 的电离程度小于AsO
的电离程度小于AsO![]() 的水解程度,Na2HAsO4溶液显碱性,c(H2AsO
的水解程度,Na2HAsO4溶液显碱性,c(H2AsO![]() )>c(AsO
)>c(AsO![]() ),同时水也电离出氢氧根离子,故c(Na+)>c(HAsO
),同时水也电离出氢氧根离子,故c(Na+)>c(HAsO![]() )>c(OH-)>c(H2AsO
)>c(OH-)>c(H2AsO![]() )>c(AsO
)>c(AsO![]() ),B正确;
),B正确;
C.向H3AsO4溶液滴加NaOH溶液至中性,溶液中存在[H+]=[OH-]、c(HAsO![]() )=c(H2AsO
)=c(H2AsO![]() ),根据电荷守恒c(Na+)=2c(HAsO
),根据电荷守恒c(Na+)=2c(HAsO![]() )+ c(H2AsO
)+ c(H2AsO![]() ),C错误;
),C错误;
D.当pH=11.5时,c(HAsO![]() )=c(AsO43-),求得
)=c(AsO43-),求得![]() ,则AsO43-第一步水解的平衡常数
,则AsO43-第一步水解的平衡常数![]() ,数量级为10-3,D正确;
,数量级为10-3,D正确;
答案选C。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】化合物G是一种重要的有机产品,其合成路线如下:
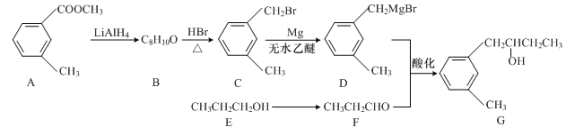
(1)E→F的反应还需的反应物和反应条件为_____。
(2)B的结构简式是_____。
(3)写出同时满足下列条件的A的一种同分异构体的结构简式:_______。
①分子中有4种不同化学环境的氢;
②能发生银镜反应和水解反应,且1mol该物质最多能与2mol NaOH反应。
(4)写出以![]() 和CH3CHO为原料,制备
和CH3CHO为原料,制备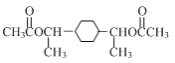 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。_____
的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲元素的原子序数是19,乙元素原子核外有两个电子层,最外电子层上有6个电子;丙是元素周期表第ⅠA族中金属性最弱的碱金属元素。由此推断:
(1)甲元素在周期表中位于第_______周期;乙元素在周期表中位于第______族;丙元素的名称为________。
(2)甲的单质与水反应的离子方程式为____________________________,乙单质与丙单质反应的化学方程式为____________________________________,甲的单质与水反应的生成物的电子式为:_______________,___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是优良的多功能、绿色水处理剂。制备高铁酸钾的装置如图:
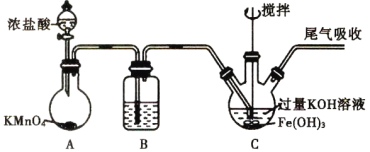
资料:①K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在0℃~5℃、强碱性溶液中比较稳定。②制备K2FeO4的反应为放热反应。下列叙述正确的是
A.装置A中的KMnO4可以用MnO2代替
B.装置B中的试剂为饱和碳酸氢钠溶液,目的是除去C12中的HC1
C.装置C中生成K2FeO4的关键操作是要缓慢通入Cl2且不能过量
D.K2FeO4做水处理剂时能杀菌消毒、吸附悬浮物与Cl2作用相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO, MgSO3(s) + CO(g)![]() MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是

选项 | x | y |
A | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
C | SO2的浓度 | 平衡常数K |
D | MgSO4的质量(忽略体积) | CO的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验与图象对应的是
选项 | A | B | C | D |
实验 | NaAlO2溶液中逐滴滴加盐酸至过量 | AlCl3溶液中逐滴滴加氨水至过量 | 明矾溶液中逐滴滴加Ba(OH)2溶液至过量 | 澄清石灰水中缓慢通入CO2至过量 |
图象 |
|
|
|
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有H+、Mg2+、Al3+三种阳离子,逐滴加入1mol/LNaOH溶液,消耗NaOH溶液体积和生成沉淀之间的关系如图所示,则下列说法正确的是( )
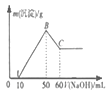
A.横坐标0-50mL时,发生反应只有:Mg2++2OH-═Mg(OH)2↓,Al3++3OH-═Al(OH)3↓
B.B点生成沉淀的物质的量为0.02mol
C.若往C点的溶液中加入0.1mol/L盐酸50mL,沉淀将全部溶解
D.H+、Mg2+、Al3+三种阳离子物质的量浓度之比为2:1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2![]() 2NO+O2在密闭容器反应,达到平衡状态的标志是()
2NO+O2在密闭容器反应,达到平衡状态的标志是()
(1)单位时间内生成n mol O2的同时生成2n mol NO2
(2)单位时间内生成n mol O2的同时生成2n mol NO
(3)用NO2、NO、O2的物质的量浓度变化表示反应速率的比为2:2:1的状态
(4)混合气体的颜色不再改变的状态
(5)混合气体的平均相对分子质量不再改变的状态.
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某简单(单核)粒子的原子核外有10个电子。
(1)若为原子,请画出其原子结构示意图______________。
(2)若为阳离子,请写出其常见的离子符号______________。
(3)若为阴离子,请写出其常见的离子符号______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com