
(1)室温下在pH=12的NaCN溶液中,由水电离的c(OH—)为 mol?L—1。
(2)浓度为0.1mol?L—1的下列各物质的溶液中,c(NH4+)由大到小的顺序是___(填序号)。
①NH4Cl ②NH4HSO4 ③NH3?H2O ④CH3COONH4
(3)某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A=H+ +HA—,HAˉ H+ +A2—。
H+ +A2—。
①则Na2A溶液显____性;NaHA溶液显 性(填“酸性”、“中性”或“碱性”)。
②若有0.1mo1?L—1Na2A的溶液,其中各种离子浓度由大到小的顺序是: (填序号)。
| A.c(Na+)>c(A2—)>c(OH—)>c(HA—)>c(H+) |
| B.c(Na+)> c(OH—)>c(HA—)> >c(A2—) > c(H+) |
| C.c(Na+)> c(H+)> c(A2—)> c(OH—)>c(HA—) |
| D.c(A2—)>c(Na+)> c(OH—) > c(H+)>c(HA—) |
(1)10—2(1分)
(2)②>①>④>③(2分)
(3)①碱性(1分) 酸性(1分)②A(2分)
(4)①4.1×10—14mo1/L(2分) ②是(1分)
解析试题分析:(1)NaCN是强碱弱酸盐,则水电离的c(OH—)=c(OH—)=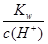 =10—2mol/L;(2)NH3?H2O的电离程度最小,则其所含c(NH4+)最小;HSO4—或H+能抑制NH4+的水解,则NH4HSO4溶液中c(NH4+)最大;CH3COO—能促进NH4+的水解,则CH3COONH4溶液中c(NH4+)比NH4Cl溶液小;(3)由于A2—+H2O
=10—2mol/L;(2)NH3?H2O的电离程度最小,则其所含c(NH4+)最小;HSO4—或H+能抑制NH4+的水解,则NH4HSO4溶液中c(NH4+)最大;CH3COO—能促进NH4+的水解,则CH3COONH4溶液中c(NH4+)比NH4Cl溶液小;(3)由于A2—+H2O HAˉ+OHˉ,则Na2A溶液显碱性;由于HAˉ
HAˉ+OHˉ,则Na2A溶液显碱性;由于HAˉ H+ +A2—,则NaHA溶液显酸性;Na2A=2Na++A2—,A2—+H2O
H+ +A2—,则NaHA溶液显酸性;Na2A=2Na++A2—,A2—+H2O HAˉ+OHˉ,H2O
HAˉ+OHˉ,H2O H+ +OH—,由电离、水解原理可知,c(Na+)>c(A2—)>c(OH—)>c(HA—)>c(H+),故选A;(4)由于c(Ag+)?c(Br—)=Ksp(AgBr),则c(Ag+)=
H+ +OH—,由电离、水解原理可知,c(Na+)>c(A2—)>c(OH—)>c(HA—)>c(H+),故选A;(4)由于c(Ag+)?c(Br—)=Ksp(AgBr),则c(Ag+)= =4.1×10—14mo1/L;c(Ag+)?c(Cl—)=Ksp(AgCl),则c(Ag+)=
=4.1×10—14mo1/L;c(Ag+)?c(Cl—)=Ksp(AgCl),则c(Ag+)=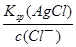 =1.6×10—9mo1/L,此时Qc(AgI)=c(Ag+)?c(I—)=1.6×10—10>Ksp(AgI),Qc(AgBr)=c(Ag+)?c(Br—)=1.6×10—10>Ksp(AgBr),则Br—、I—已经沉淀完全。
=1.6×10—9mo1/L,此时Qc(AgI)=c(Ag+)?c(I—)=1.6×10—10>Ksp(AgI),Qc(AgBr)=c(Ag+)?c(Br—)=1.6×10—10>Ksp(AgBr),则Br—、I—已经沉淀完全。
考点:考查水的离子积、溶液的pH和酸碱性、盐类水解、溶液中离子浓度大小比较、溶度积、沉淀的生成等相关知识。


科目:高中化学 来源: 题型:填空题
以下是25℃时几种难溶电解质的溶解度:
| 难容电解质 | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶解度/g | 9×10-4 | 1.7×10-6 | 1.5×10-4 | 3.0×10-9 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
SiO2、SO2和CO2都是酸性氧化物,它们的化学性质有一定的相似性;Mg和Na的化学性质也有一定相似性。某兴趣小组用如图所示装置进行Mg与SO2反应的实验。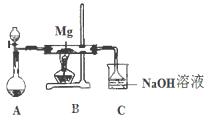
(1)选择制取SO2的合适试剂 (填编号)。
①浓HCl ②浓H2SO4
③Na2SO3固体 ④CaSO3固体
(2)上述装置还可优化,优化的方法是 ,实验后装置C中所得溶液离子浓度关系一定正确的是(选填字母)
| A.(Na+)= 2c(SO32-)+ c(HSO3-), |
| B.(Na+)> c(HSO3-)> c(SO32-)> c(H+)> c(OH-), |
| C.(H2SO3)+ c(H+)= c(SO32-)+ (OH-), |
| D.(Na+)+ c(H+)=" 2" c(SO32-)+ c(HSO3-)+ c(OH-) |
 2MgSO3+S;
2MgSO3+S; 2MgO+MgS,
2MgO+MgS,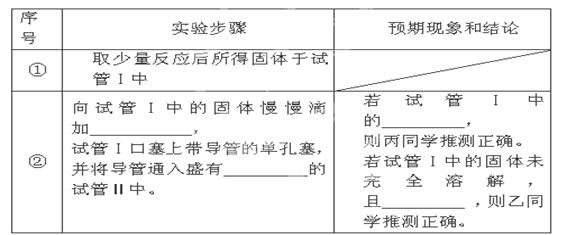
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有25 ℃时0.1 mol·L-1的氨水,请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,一水合氨的电离平衡________(填“向左”、“向右”或“不”)移动;此时溶液中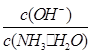 ________(填“增大”、“减小”或“不变”)。
________(填“增大”、“减小”或“不变”)。
(2)若向氨水中加入等浓度稀醋酸,使其恰好中和,写出反应的离子方程式:_________________;所得溶液的pH________7(填“>”、“<”或“=”),
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时[NH4+]=a mol·L-1,则c(SO42-)=________。
(4)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子的物质的量浓度由大到小的顺序是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
常温下,有浓度均为1 mol·L-1的下列4种溶液:
①H2SO4溶液 ②NaHCO3溶液 ③NH4Cl溶液 ④NaOH溶液
(1)这4种溶液pH由大到小的顺序是 ,其中由水电离的H+浓度最小的是 。(均填序号)
(2)②中各离子浓度由大到小的顺序是 ,NaHCO3的水解平衡常数Kh= mol·L-1。(已知碳酸的电离常数K1=4×10-7,K2=5.6×10-11)
(3)向③中通入少量氨气,此时 的值 (填“增大”、“减小”或“不变”)。
的值 (填“增大”、“减小”或“不变”)。
(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积 ④的体积(填“大于”、“小于”或“等于”之一)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
向2支盛有1 mL 1 mol·L-1的MgCl2溶液中各加入10滴2 mol·L-1 NaOH,制得等量Mg(OH)2沉淀;然后分别向其中加入不同试剂,记录实验现象如下表:
| 实验序号 | 加入试剂 | 实验现象 |
| Ⅰ | 4 mL 2 mol·L-1 HCl 溶液 | 沉淀溶解 |
| Ⅱ | 4 mL 2 mol·L-1 NH4Cl 溶液 | 沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。请根据所学的知识回答:下表是不同温度下水的离子积数据:
| 温度 / ℃ | 25 | t1 | t2 |
| 水的离子积常数 | 1×10-14 | α | 1×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离。但事实是,硫酸在水中的第一步电离是完全的,第二步电离并不完全,其电离情况为:
H2SO4=H++HSO4-,HSO4- H++SO42-。
H++SO42-。
请回答下列有关问题:
(1)K2SO4溶液呈 ____________ (填“弱酸性”、“中性”或“弱碱性”),其理由是_____________________________(用离子方程式表示)。
(2)NaHSO4溶液与NaHCO3溶液反应的离子方程式为________________________________。
(3)若25℃时,0.10 mol·L-1的NaHSO4溶液中c(SO42-)="0.029" mol·L-1,则HSO4-的电离常数Ka="____________" (保留两位有效数字);0.10 mol·L-1的H2SO4溶液中c(H+)____________ 0.129mol·L-1(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
为了证明醋酸是弱电解质,甲、乙、丙、三人分别选用下列试剂进行实验:
0.1 mol·L-1醋酸溶液、pH=3的盐酸、pH=3的醋酸、、蒸馏水、锌粒、pH试纸等。
(1)甲取出10 mL0.1 mol·L-1醋酸溶液,用pH试纸测出其pH=a,确定醋酸是弱电解质,则a应该满足的关系是_________,理由是__________________________________。
(2)乙将pH=3醋酸和盐酸,各取1 mL,用蒸馏水稀释到100 mL,然后用pH试纸
分别测定两溶液的pH,则可认定醋酸是弱电解质,判断的依据是______________________________。
(3)丙分别取pH=3的盐酸和醋酸10 mL,然后分别加入质量相同的锌粒,醋酸放出H2的平均速率 (填“快”或“慢”),则认定醋酸是弱电解质,。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com