
分析 (1)电解质:在水溶液中或熔融状态下能够导电的化合物;非电解质:在熔融状态和水溶液中都不能导电的化合物;
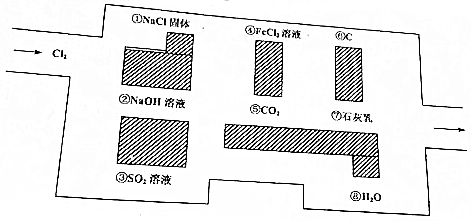
(2)解决该题应该找出一条不能和氯气发生反应的物质构成的路;
(3)氯气具有强氧化性,可与氢氧化钠溶液、二氧化硫、氯化亚铁溶液、石灰乳、水反应;
(4)氢氧化钠溶液,不与氯化钠固体、氢氧化钠溶液、水反应分析判断.
解答 解:(1)①氯化钠固体在水溶液中或熔融状态下能够导电,属于电解质;
②③④都是混合物,既不是电解质也不是非电解质;
⑤二氧化碳自身不能电离,属于非电解质;
⑥C为单质,既不是电解质也不是非电解质;
⑦石灰乳是混合物,既不是电解质也不是非电解质;
⑧水在水溶液中能够导电,属于电解质;
故属于电解质的是①⑧;属于非电解质的是⑤;
故答案为:①⑧;⑤;
(2)利用图示的物质对相关的与氯气不能反应的物质作出判断即可,由于氯气不能和氯化钠固体、二氧化碳、碳等反应,所以走出迷宫表示所走的路线为①→⑤→⑥,故答案为:①→⑤→⑥;
(3)氯气具有强氧化性,可与氢氧化钠溶液、二氧化硫、氯化亚铁溶液、石灰乳、水反应并且都是氧化还原反应,则属于氧化还原反应的有5个,既属于氧化还原反应又属于化合反应的化学方程式为Cl2+2FeCl2═2FeCl3,故答案为:Cl2+2FeCl2═2FeCl3;
(4)氢氧化钠溶液,不与氯化钠固体、氢氧化钠溶液、水反应,则能走出迷宫,故答案为:能;氢氧化钠溶液,不与氯化钠固体、氢氧化钠溶液、水反应.
点评 本题考查物质的性质,为高频考点,综合考查元素化合物知识,把握金属及化合物的性质、反应类型及发生的反应为解答的关键,侧重分析能力及知识的应用能力和解决问题的能力的考查,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | H2→H+H的过程需要吸收热量 | |
| B. | 若生成2mol水蒸气,则放出的能量大于566 kJ | |
| C. | 2g氢气完全燃烧生成液态水所释放的能量为283kJ | |
| D. | 2mol氢气与1mol氧气的能量之和大于2mol液态水的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
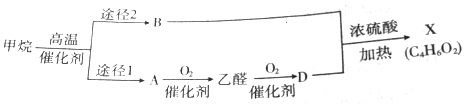
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | Al(OH)3与过量NaOH溶液反应:Al(OH)3+OH-═AlO2-+2H2O | |
| C. | Al(OH)3与过量盐酸反应:Al(OH)3+H+═Al3++3H2O | |
| D. | AlCl3溶液中加入过量NaOH溶液:Al3++4OH-═AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铵态氮肥不能与草木灰混合使用 | |
| B. | 大力推进小火力发电站的兴建,以缓解地方用电困难 | |
| C. | 医学上,常使用BaSO4做内服造影剂 | |
| D. | 为防止电池中重金属等污染环境和水体,应积极开发废旧电池的综合技术 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Ca2+、Cl-、SO42- | B. | Al3+、Na+、SO32-、HCO3- | ||
| C. | Mg2+、NH4+、Cl-、SO42- | D. | K+、Fe3+、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氮的固定是指气态氮变为固态 | |
| B. | “歼-20”飞机上使用的碳纤维是一种新型的有机高分子材料 | |
| C. | 利用二氧化碳制造全降解塑料,可以缓解温室效应 | |
| D. | 石油分馏、煤的干馏、蛋白质的变性和纳米银粒子的聚集都是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com