
| A、小苏打可与酸反应,可用作治疗胃酸过多的药剂 | B、氯化铝是电解质,可电解其水溶液获得金属铝 | C、SO2具有漂白性,可用于将银耳漂白为“雪耳” | D、二氧化硅具有导电性,可用于生产光导纤维 |


 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
| A、①④⑤⑥ | B、①②③④⑤ | C、①④ | D、①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、拒绝脂肪 | B、对蛋白质要“亲疏有度” | C、科学饮食从“微量”元素做起 | D、饮食中不可缺“肠道的清道夫--纤维素” |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CsOH在水溶液中的电离方程式为CsOH═Ca++OH- | B、CsOH溶液能使酚酞试液变红 | C、因为CsCl是易溶于水的盐,所以CsOH溶液与稀盐酸不发生复分解反应 | D、CsOH溶液与MgCl2溶液发生复分解反应,有氢氧化镁沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
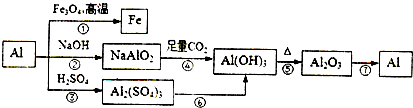
| A、反应①又称铝热反应,可用于野外焊接铁轨 | B、反应②、③都有氢气生成,产生等量的氢气时转移的电子数相等 | C、常用反应⑥制备Al(OH)3,方法是向Al2(SO4)3溶液中滴加足量的NaOH溶液 | D、工业上用反应⑦制备铝时,常加入冰晶石以降低氧化铝的熔融温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、非金属元素组成的化合物中可能含离子键 | B、ⅠA族金属元素是同周期中金属性最强的元素 | C、同种元素的原子均有相同的质子数 | D、ⅦA族元素的阴离子还原性越强,其氢化物越稳定 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省海珠等四区高三联考理综化学试卷(解析版) 题型:填空题
(16分)合成喹啉及其衍生物常用的方法是Skraup合成法,以下是用苯胺、甘油、浓硫酸和硝基苯共热制备喹啉的反应流程。
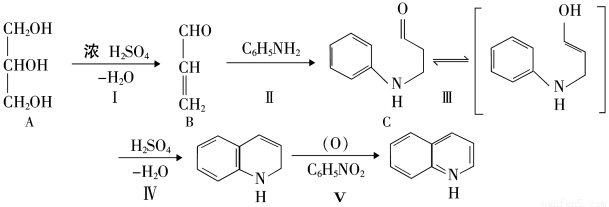
(1)上图中A的名称为 ,C的分子式为
(2)II的反应类型为
(3)下列关于化合物C的说法,正确的是
A.1mol化合物C最多能与3mol氢气反应
B.可发生银镜反应
C.能使酸性高锰酸钾溶液褪色
D.属于芳香烃
(4)①化合物E和F也能发生类似II的反应,请写出生成物的结构简式。
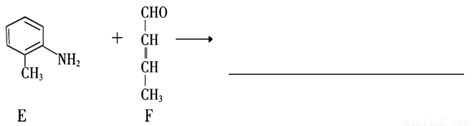
②化合物F有多种同分异构体,其中属于醛类的有(不包括该物质本身) (写结构简式)
查看答案和解析>>
科目:高中化学 来源:2015届广东省广州市高三9月第二次月考化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值。下列说法正确的是
A.标况下,11.2L SO3所含的分子数目为0.5 NA
B.室温下,1L pH=1的稀硫酸溶液中,由水电离的H+离子数目为0.2NA
C.铅蓄电池放电时,正极消耗4mol H+,则电路中通过的电子数目为2NA
D.8 Al + 3NH4ClO4 =4 Al2O3 +3NH3 +3HCl 反应中,消耗27gAl粉时,转移的电子数目为2.75NA(Al原子量—27)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com