
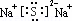
分析 (1)W、X是金属元素,W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,则W为Na,X为Al;
(2)W与Y可形成化合物W2Y,则Y是非金属硫,该化合物为硫化钠;
(3)硝酸铝为强酸弱碱盐,铝离子部分水解,溶液显酸性;
(4)Y、Z是非金属元素,Y的低价氧化物通入Z单质的水溶液中,则Z为Cl,二氧化硫和氯气反应生成盐酸与硫酸;
(5)Z的最高价氧化物为无色液体,为Cl2O7,0.25mol该物质与一定量水混合得到一种稀溶液,并放出Q kJ的热量,则1molCl2O7与水反应放出4DkJ的热量;
(6)Z为Cl,质子数数为17,质子数比中子数少3,则中子数为20,质量数为37;
(7)W为Na,对应的最高价氧化物的水化物为NaOH.
解答 解:(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,则W是金属钠,X是金属铝,氢氧化铝是两性氢氧化物,能和强碱反应生成盐和水,该反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(2)W与Y可形成化合物W2Y,则Y是非金属硫,硫化钠使钠离子和硫离子间通过离子键形成的离子化合物,电子式为: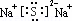 ,
,
故答案为: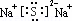 ;
;
(3)X为Al,其硝酸盐为硝酸铝,铝离子在溶液中部分水解:Al3++3H2O═Al(OH)3+3H+,溶液显示酸性,
故答案为:酸;Al3++3H2O═Al(OH)3+3H+;
(4)Y、Z是非金属元素,Y的低价氧化物通入Z单质的水溶液中,则Z为Cl,二氧化硫和氯气反应生成盐酸与硫酸,该反应为:SO2+C12+2H2O═H2SO4+2HCl,
故答案为:SO2+C12+2H2O═H2SO4+2HCl;
(5)Z的最高价氧化物C12O7为无色液体,0.25mol该物质与一定量水混合得到HClO4的水化物的稀溶液,并放出Q kJ的热量,则1mol Cl2O7反应放出的热量为4QkJ,故该反应的热化学方程式为:Cl2O7(l)+H2O(l)═2HClO4(aq)△H=-4QkJ•mol-1,
故答案为:Cl2O7(l)+H2O(l)═2HClO4(aq)△H=-4QkJ•mol-1;
(6)Z为Cl,质子数数为17,质子数比中子数少3,则中子数为20,质量数为37,可表示为3717Cl,故答案为:3717Cl;
(7)W为Na,对应的最高价氧化物的水化物为NaOH,含有离子键、极性共价键,故答案为:离子键、极性共价键.
点评 本题考查位置、结构、性质的关系的综合应用,题目难度中等,熟悉第三周期元素的性质变化规律及常见元素的单质和化合物的性质是解答本题的关键,试题培养了学生灵活应用基础知识解决实际问题的能力.


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:推断题
| 单质 | A | B | C | D | E |
| 最高价氧化物 对应水化物的稳定性 | 难分解 | 能分解 | 能分解 | 能分解 | 能分解 |
| 单质性质 | 与水剧烈反应 | 缓慢溶于热水 | 溶于强碱性溶液 | 难溶于冷的浓硝酸 | 溶于浓、稀硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
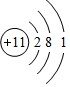 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
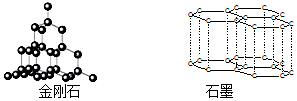
| A. | 根据:C(金刚石,s)+O2(g)═CO2(g)△H=-395.41 kJ•mol-1C(石墨,s)+O2(g)═CO2(g)△H=-393.5 kJ•mol-1说明金刚石比石墨稳定,石墨转变为金刚石为放热反应 | |
| B. | 相同质量的金刚石与石墨晶体中,所含共价键数相同 | |
| C. | 估计金刚石与石墨的熔沸点均较高,硬度均较大 | |
| D. | 现代科技已经实现了石墨制取金刚石,该过程属于化学变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com