
能正确表示下列化学反应的离子方程式是 ( )
A.氢氧化钡与硫酸反应:OH?+H+==H2O
B.NaOH溶液中通入少量二氧化碳:CO2+OH?==HCO3-
C.氧化铁与盐酸混合:Fe2O3+6H+==2Fe3++3H2O
D.CH3COOH溶液与NaOH溶液反应:OH?+H+==H2O
科目:高中化学 来源:2015-2016学年云南省高一下期末化学试卷(解析版) 题型:选择题
下列叙述或实验现象描述正确的是( )
A. 将铜与浓硫酸共热,产生使石蕊溶液变红的气体,说明浓硫酸具有酸性
B. 往足量铁与稀硝酸反应后的溶液中滴入KSCN溶液,溶液变为血红色
C. 往FeSO4溶液中通入NO2气体,溶液始终无明显现象
D. 往BaCl2溶液中通入SO2气体,无沉淀产生,再通NH3,产生白色沉淀
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高二下期末化学试卷(解析版) 题型:选择题
常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A.使酚酞变红色的溶液中:Na+、Al3+、SO42﹣、Cl﹣
B.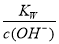 =1×10﹣13molL﹣1的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
=1×10﹣13molL﹣1的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
C.与Al反应能放出H2的溶液中:Fe2+、K+、NO3﹣、SO42﹣
D.水电离的c(H+)=1×10﹣13molL﹣1的溶液中:K+、Na+、AlO2﹣、CO32﹣
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高一下期末化学试卷(解析版) 题型:选择题
向a mL0.25mol·L-1的AlCl3溶液中加入金属钠,反应完全后,恰好只形成NaCl和NaAlO2的混合溶液,则加入金 属钠的物质的量为( )
属钠的物质的量为( )
A.2.5a×10-4mol B.a×10-3mol C.7.5a×10-4mol D.a×10-4mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高一下期末化学试卷(解析版) 题型:选择题
下列叙述中不正确的是( )
A. 用石墨作电极电解CuSO4溶液,通电一段时间后,在标准状况下两极产生的气体可能相等
B. 船底镶嵌锌块,锌作负极,以防船体被腐蚀
C. 钢铁吸氧腐蚀的正极反应:O2+2H2O+4e-===4OH-
D. 电解池中的阳极和原电池中的负极上都发生还原反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高二上期末化学试卷(解析版) 题型:填空题
Ⅰ.CO可用于合成甲醇。在压强为0.1MPa条件下,在体积为bL的密闭容器中充入a mol CO和2a mol H2,在催化剂作用下合成甲醇:
CO(g)+2H2(g) CH3OH(g)平衡时CO的转化率与温度、压强的关系如下图:
CH3OH(g)平衡时CO的转化率与温度、压强的关系如下图:
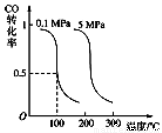
(1)该反应属于 反应(填“吸热”或“放热”)。
(2)100℃时,该反应的平衡常数:K= (用a、b 的代数式表示)。
(3)在温度和容积不变的情况下,再向平衡体系中充入a mol CO,2a mol H2,达到平衡时CO转化率
(填“增大”“不变”或“减小”)
Ⅱ.T ℃时,纯水中c(OH-)为10-6 mol·L-1,则该温度时
(1)将pH=3 的H2SO4溶液与pH=10的NaOH溶液按体积比9:2 混合,所得混合溶液的pH为 。
(2)若1体积pH1=a的某强酸溶液与10体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 。
Ⅲ. 在25mL的氢氧化钠溶液中逐滴加入0. 2 mol/ L醋酸溶液,滴定曲线如图所示。

(1)该氢氧化钠溶液浓度为________________。
(2)在B点,a_________12.5 mL(填“<”“>”或“=”)。
(3)在D点,溶液中离子浓度大小关系为_____________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高二上期末化学试卷(解析版) 题型:选择题
电子表所用的某种纽扣电池的电极材料为Zn和Ag2O,电解质溶液是KOH溶液。电池总反应式为:Zn+Ag2O=ZnO+2Ag,下列说法错误的是( )
A.该电池工作时,电解质中的阴离子向负极移动
B.该电池负极的电极反应式为:Zn+2OH--2e-=ZnO+H2O
C.理论上该电池工作一段时间后,溶液中KOH的浓度不变
D.该电池的正极是Zn,负极是Ag2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高一下期末化学试卷(解析版) 题型:实验题
乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验可用a装置来制备。
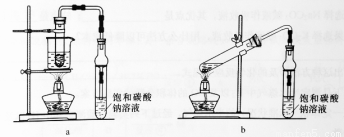
完成下列填空:
(1)实验时,通常加入过量的乙醇,原因是______________。加入数滴浓硫酸即能起催化作用,但实际用量多于此量,原因是_______________;浓硫酸用量又不能过多,原因是____________。
(2)饱和Na2CO3溶液的作用是_______________。
(3)反应结束后,将试管中收集到的产品倒入分液漏斗中,_________、________,然后分液。
(4)若用b装置制备乙酸乙酯,其缺点有__________、__________。由b装置制得的乙酸乙酯产品经饱和碳酸钠溶液和饱和食盐水洗涤后,还可能含有的有机杂质是________,分离乙酸乙酯与该杂质的方法是_______________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二下期末化学试卷(解析版) 题型:选择题
某元素+3价离子的电子排布式为1s22s22p63s23p63d5,则该元素在周期表中的位置为( )
A. ⅤB族 B. ⅢB族 C. Ⅷ族 D. ⅤA族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com