

| A. | ①②中Mg作负极,③④中Fe作负极 | |
| B. | ②中Mg作正极,电极反应式为:2H2O+2e-═2OH-+H2↑ | |
| C. | ③中Fe作负极,电极反应式为Fe-2e-═Fe2+ | |
| D. | ④中Cu作正极,电极反应式为2H++2e-═H2↑ |
分析 A、根据氧化还原反应,失电子的极是负极;
B、原电池的正极发生得电子的还原反应;
C、铜作负极发生氧化反应;
D、铁、铜、氯化钠构成的原电池中,金属铁发生的是吸氧腐蚀.
解答 解:A、②中的氧化还原反应发生在金属铝和氢氧化钠之间,失电子的是金属铝,为负极,③中金属铁在常温下遇浓硝酸钝化,不能形成原电池,故A错误;
B、②中的氧化还原反应发生在金属铝和氢氧化钠之间,失电子的是金属铝,为负极,Mg作为正极,电极反应式为2H2O+2e-═2OH-+H2↑,故B正确;
C、③中铜作负极发生氧化反应,所以铜失电子生成铜离子,即电极反应式为Cu-2e-═Cu2+,故C错误;
D、铁、铜、氯化钠构成的原电池中,金属铁为负极,金属铜为正极,铁发生的是吸氧腐蚀,正极上是氧气得电子的过程,故D错误.
故选B.
点评 本题考查学生原电池的工作原理知识,电极的活泼性与电解质溶液有关,如镁和铝在氢氧化钠溶液中铝活泼而铁与铜在冷的浓硫酸和浓硝酸中铜活泼,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 用溴水检验CH2=CH-CHO中是否含有碳碳双键 | |
| B. | 1mol醛发生银镜反应最多生成2molAg | |
| C. | 对甲基苯甲醛( )使高锰酸钾酸性溶液褪色,说明它含醛基 )使高锰酸钾酸性溶液褪色,说明它含醛基 | |
| D. | 能发生银镜反应的有机物不一定是醛类 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na与水反应 | B. | HCl分解为H2和Cl2 | ||
| C. | 电解Al2O3得到Al和O2 | D. | Ba(OH)2•8H2O与NH4Cl晶体混合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由Fe、Cu、FeCl3溶液组成原电池,负极反应式为:Cu-2e-═Cu2+ | |
| B. | 由Al、Cu、稀硫酸组成原电池,负极反应式为:Al-3e-═Al3+ | |
| C. | 由Al、Mg、NaOH溶液组成原电池,负极反应式为:Al+4OH--3e-═AlO2-+2H2O | |
| D. | 由Al、Cu、浓硝酸组成的原电池中,负极反应式为:Cu-2e-═Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH═CH2+Br2(水溶液)-→CH2BrCH═CH2+HBr | |
| B. | nCH3CH═CH2$\stackrel{一定条件下}{→}$[CH3-CH-CH2]n | |
| C. | CH2═CH-CH═CH2+Br2-→CH2Br2-CH═CH-CH3 | |
| D. | CH3CH2OH$\stackrel{浓H_{2}SO_{4}}{→}$CH2═CH2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
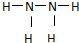 ,过氧化氢的电子式
,过氧化氢的电子式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2、Cl2均能使品红溶液褪色 | |
| B. | NH4Cl晶体、固态碘受热时均能变成气体 | |
| C. | 苯酚,乙烯均能使溴水褪色 | |
| D. | 福尔马林,葡萄糖与新制的Cu(OH)2共热均有红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知t℃、p kPa时,在容器甲和容器乙中分别充入1 mol A(g)和1 mol B(g),发生反应A(g)+B(g)?C(g)△H<0,反应过程中温度保持不变.已知起始时V乙=$\frac{5}{7}$V甲,装置如图所示,当反应达平衡时,测得甲中C的体积分数为40%,下列说法不正确的是( )
已知t℃、p kPa时,在容器甲和容器乙中分别充入1 mol A(g)和1 mol B(g),发生反应A(g)+B(g)?C(g)△H<0,反应过程中温度保持不变.已知起始时V乙=$\frac{5}{7}$V甲,装置如图所示,当反应达平衡时,测得甲中C的体积分数为40%,下列说法不正确的是( )| A. | 容器甲乙中反应的平衡常数相等 | |
| B. | 容器甲乙中反应的起始速率不等 | |
| C. | 达平衡时,容器甲、乙中各组分的体积分数不等 | |
| D. | 达平衡时,容器甲、乙中放出的热量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com