
| V |
| Vm |
| V |
| Vm |
| 67.2L |
| 22.4L/mol |
| 1 |
| 1+2 |
| 1 |
| 3 |
| 1 |
| 3 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下在pH=1的溶液中:NH4+、K+、HCO3-、Cl- |
| B、有SO42-存在的溶液中:Na+、Mg2+、Ca2+、I- |
| C、有NO-3存在的强酸性溶液中:NH+4、Ba2+、Fe2+、Br- |
| D、常温下在pH=13的溶液中:Na+、S2-、PO43-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 26g |
| 100g |
| A、△H-T△S<0△S<0 |
| B、△H-T△S<0△S>0 |
| C、△H-T△S>0△S>0 |
| D、△H-T△S>0△S<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 纯净物 | 混合物 | 电解质 | 非电解质 | |
| A | 盐酸 | 水煤气 | 硫酸 | 铜 |
| B | 胆矾 | 石灰水 | 硫酸钡 | NH3 |
| C | 火碱 | 蔗糖溶液 | 氯化钠溶液 | 三氧化硫 |
| D | 冰醋酸 | 氢氧化铁胶体 | 苛性钾溶液 | 乙醇 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
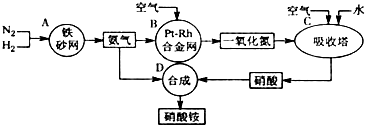
查看答案和解析>>
科目:高中化学 来源: 题型:
| 加入试剂 | 0.1mol/LH2C2O4溶液 | 0.2mol/LH2C2O4溶液 |
| 实验现象 | ||
| 褪色时间 | 16s | 9s |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com