
【题目】某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。 [制取氨气的反应原理: 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O]
CaCl2+2NH3↑+2H2O]

【实验探究】
(1) 利用上述原理,实验室制取氨气应选用下图中_______________发生装置进行实验。

(2)B 装置中的干燥剂可选用______________(填“碱石灰”或“浓硫酸”)。
(3)用 5.35 g NH4Cl 固体与足量 Ca(OH)2 反应,最多可制得标准状况下氨气的体积为 _________L。( NH4Cl 的摩尔质量为 53.5 g·mol-1)
(4)气体通过 C、D 装置时,试纸颜色会发生变化的是 __________( 填“C”或“D”)。
(5)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2 滴浓盐酸,可观察到的现象是______________。
(6)F装置中倒置漏斗的作用 _____________。
(7)某同学用氨气和滴加酚酞的水做喷泉实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有________性质(填序号)。
a.还原性 b.极易溶于水 c.与水反应生成碱性物质
(8)氨气的用途很广。如可用氨气处理二氧化氮: 8NH3 + 6NO2 =7N2 + 12H2O该反应中氨气体现________( 填“氧化性”或“还原性”)。请你列举出氨气的另一种用途__________。
【答案】(12分)(1)a(1分)(2)碱石灰(1分)(3)2.24(2分)
(4)D(1分)(5)产生白烟(1分)(6)防止倒吸(1分)
(7)bc(说明:若只选b或只选c给1分,其它只要出现a不给分)……(2分)
(8)还原性(1分)①致冷剂②氮肥(或化肥)的原料③硝酸的原料④化工原料
(以上任选其一,或其它合理答案也给分) (1 分)
【解析】
试题分析:(1) 固体混合加热,可选择a发生装置进行实验;
(2)干燥管内盛放的是固体干燥剂,则干燥氨气可选用碱石灰;
(3)n(NH4Cl)=5.35g÷53.5g·mol-1=0.1mol,
根据反应方程式可知,n(NH3)=n(NH4Cl)=0.1mol,
所以V(NH3)=nVm=0.1mol×22.4L/mol=2.24L;
(4)氨气能使湿润的红色石蕊试纸变蓝,所以D中颜色发生变化;
(5)氨气与挥发的HCl会生成氯化铵晶体,所以有白烟生产;
(6)氨气极易溶解于水,利用F装置中倒置漏斗可防倒吸;
(7)利用氨气和滴加酚酞的水做喷泉实验,烧瓶内产生红色喷泉的现象,说明氨气极易溶于水且氨气与水反应生成碱性物质,答案为bc;
(8)在8NH3 + 6NO2 =7N2 + 12H2O反应中氨气中氮元素化合价升高,被氧化,体现还原性,氨气常见用途有①致冷剂②氮肥(或化肥)的原料③硝酸的原料④化工原料等。


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
【题目】做实验时不小心使皮肤上粘了一些高锰酸钾,形成的黑斑很久才能消除,如果用草酸(乙二酸)的稀溶液洗涤,黑斑可以迅速退去,其离子方程式为(未配平):
MnO4-+H2C2O4+H+→CO2+Mn2++![]() ,下列有关叙述正确的是
,下列有关叙述正确的是
A.该反应的氧化剂为H2C2O4
B.该离子方程式右侧方框内的产物是OH-
C.6mol H+参加反应时,电子转移10mol
D.每生成1mol CO2,电子转移的数目为1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 13C﹣NMR(核磁共振)、15N﹣NMR可用于测定蛋白质、核酸等生物大分子的空间结构,这项研究曾获2002年诺贝尔化学奖.下面有关叙述正确的是( )
A.13C与15N有相同的中子数
B.13C与C60互为同素异形体
C.15N 与14N 互为同位素
D.232Th转化成233U是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水(酸性)中的有机物可用C6H10O5表示[交换膜分别是只允许阴(阳) 离子通过的阴(阳)离子交换膜],下列有关说法中不正确的是
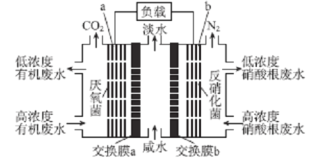
A.电池工作时,电子由a极经导线流向b极
B.交换膜a是阴离子交换膜
C.电极 b 的反应式:2NO3-+l0e-+12H+=N2↑+6H2O
D.相同时间内(相同状况下)生成CO2和N2的体积比为2:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正盐 A 能发生下图所示的反应,图中①~⑧分别代表有关反应中的一种物质(某些物质已略去),其中①、 ②、 ④、 ⑤为无色气体, ⑥为红棕色气体。(已知镁在二氧化碳气体中点燃生成碳单质和氧化镁)
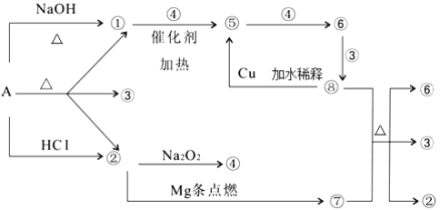
请完成下列各题:
(1)写出化学式 A__________,⑥__________,⑦_________;
(2)写出下列反应化学方程式:
⑧+⑦→②+③+⑥:_______________; ①+④→⑤:______________;
(3)⑧→⑤的离子方程式为:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如下图所示,工作原理为:Fe3++Cr2+ ![]() Fe2++Cr3+。下列说法正确的是
Fe2++Cr3+。下列说法正确的是
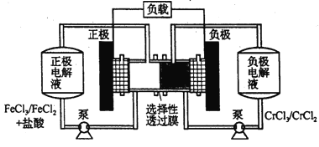
A.氧化性:Cr3+ >Fe3+
B.电池放电时,负极的电极反应式为:Fe2+-e-=Fe3+
C.充电时,阴极的电极反应式为:Cr3+ +e-= Cr2+
D.电池放电时,Cl-从负极室穿过选择性透过膜移向正极室
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】进入冬季以后,我国许多城市将出现雾霾天气,下列做法能减轻雾霾形成的是
A. 市郊露天焚烧秸秆 B. 大力推广使用燃煤发电
C. 大量使用机动车辆 D. 多利用太阳能发电
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com