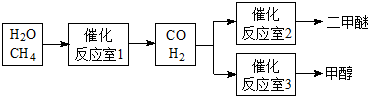
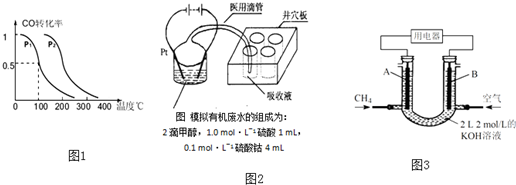
已知:在常温下,浓度均为0.1mol?L
-1的下列六种溶液的pH:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
(1)复分解反应存在这样一个规律:一种较强酸(或碱性较强的物质)可以反应生成较弱酸(或碱性较弱的物质).依照该规律,请你判断下列反应不能成立的是
(填编号).
A.CH
3COOH+Na
2CO
3═NaHCO
3+CH
3COONa
B.CH
3COOH+NaCN═CH
3COONa+HCN
C.CO
2+H
2O+2NaClO═Na
2CO
3+2HClO
D.CO
2+H
2O+2C
6H
5ONa═Na
2CO
3+2C
6H
5OH
(2)根据上表信息,写出将过量的氯气通入到少量的碳酸钠溶液中反应的离子方程式:
.
(3)根据上表信息,0.1mol?L
-1NaHCO
3溶液的pH=9.7,则溶液中c(H
2CO
3)
c(CO
32-) (填“>”、“=”或“<”),原因是
(用离子方程式和必要的文字说明).
(4)某温度下,将0.10mol CH
3COOH溶于水配成1L溶液.
①实验测得已电离的醋酸分子占原有醋酸分子总数的1.3%,求该温度下CH
3COOH的电离平衡常数K=
.(水的电离忽略不计,醋酸电离对醋酸分子浓度的影响忽略不计)
②向该溶液中再加入
mol CH
3COONa可使溶液的pH约为4.(溶液体积变化忽略不计)