
【题目】在0.1 mol·L-1NaHCO3与0.1 mol·L-1NaOH等体积混合所得的溶液中,粒子的物质的量浓度关系不正确的是( )
A.c(Na+)>c(CO32-)>c(HCO3-)>c(H2CO3)
B.c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)]
C.c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3)
D.c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-)
【答案】D
【解析】
试题分析:等体积等浓度两者发生的反应是NaHCO3+NaOH=Na2CO3+H2O,溶质为Na2CO3,属于强碱弱酸盐,A、水解程度非常微弱,溶液显碱性,CO32-+H2O![]() HCO3-+OH-,HCO3-+H2O
HCO3-+OH-,HCO3-+H2O![]() H2CO3+OH-,因此离子浓度大小顺序是c(Na+)>c(CO32-)>c(HCO3-)>c(H2CO3),故说法正确;B、根据物料守恒,c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)],故说法正确;C、根据质子守恒,c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3),故说法正确;D、根据电荷守恒,c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-),故说法错误。
H2CO3+OH-,因此离子浓度大小顺序是c(Na+)>c(CO32-)>c(HCO3-)>c(H2CO3),故说法正确;B、根据物料守恒,c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)],故说法正确;C、根据质子守恒,c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3),故说法正确;D、根据电荷守恒,c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-),故说法错误。


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源: 题型:
【题目】纯净干燥的氯气与熔融金属锡反应可制备 SnCl4,某化学小组的同学设计了如下实验装置进行制备。

已知:①金属锡熔点为 231℃,化学活泼性与铁相似;②SnCl4 的沸点为 114℃;③SnCl4 易与水反应。
请根据上图装置回答:
(1)装置Ⅳ中发生反应的化学方程式为__________________________。
(2)试管II中的试剂是___________________,装置 V 的作用是______________。
(3)裝置Ⅵ最好选用下列装置中的______________________(填标号)。

(4)实验结束后,欲回收利用装置Ⅰ中未反应完的 MnO2,需要的分离方法___________。
(5)为了顺利完成实验,点燃酒精灯的正确操作是___________________(填字母)。
A.先点燃 I 处酒精灯,后点燃Ⅳ处酒精灯
B.先点燃Ⅳ处酒精灯,后点燃 I 处酒精灯
C.同时点燃 I、Ⅳ两处酒精灯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中,不能用勒夏特列原理解释的是( )
A. 对熟石灰的悬浊液加热,悬浊液中固体质量增加
B. 实验室中常用排饱和食盐水的方式收集氯气
C. 打开汽水瓶,有气泡从溶液中冒出
D. 向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列我国科技成果所涉及物质的应用中,发生的不是化学变化的是
|
|
|
|
A.甲醇低温所制氢气用于新能源汽车 | B.氘、氚用作“人造太阳”核聚变燃料 | C.偏二甲肼用作发射“天宫二号”的火箭燃料 | D.开采可燃冰,将其作为能源使用 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的分类是学习化学的一种重要方法,科学合理的分类对于系统掌握知识、提高学习效率、解决问题都有着重要的意义。
请回答下列问题:
(1)纯净物根据其组成和性质有如图分类形式,这种分类方法层次分明、简洁直观。

①图中所示所属的分类方法为___________。
②现有碳、一氧化碳、二氧化碳、碳酸氢钠四种物质,采用下列分类标准,无法将其中两种物质归为一类的是___________________。
A.具有还原性 B.属于氧化物 C.碳元素化合价相同 D.属于电解质
③实验室常根据物质分类的原则存放药品,某学校实验室其中的四个药品柜已经存放了如下部分药品,实验室新购进一些晶体碘,应该将它存放在________________。
药品柜 | 甲柜 | 乙柜 | 丙柜 | 丁柜 |
药品 | 乙醇、乙酸 | 活性炭、红磷 | 锌粒、铜片 | 氯化钠、氯化钾 |
A.甲柜 B.乙柜 C.丙柜 D. 丁柜
④“三酸(硫酸、盐酸、硝酸)”与“两碱(氢氧化钠、碳酸钠)”能发生反应。将一定量的稀硫酸逐滴滴入到氢氧化钠和碳酸钠的混合溶液中,边滴加边搅拌,直至有少量气泡产生,此过程中共发生的离子反应有_______个。
(2)含铁元素的物质有很多,在生产、生活中应用广泛。取少量某油漆的原料Fe2O3(红棕色粉末),加人适量浓盐酸,反应后得到棕黄色溶液,取少量棕黄色溶液置于试管中再滴入NaOH溶液,可观察到有沉淀生成,生成沉淀的离子方程式为_______________________________,另在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入2 mL上述棕黄色溶液,继续加热至液体呈_______色,停止加热,证明所得分散系类型的实验方法的名称是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的转化:
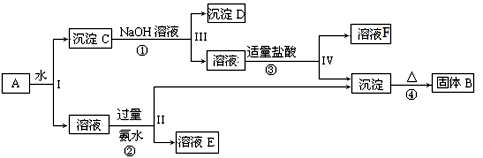
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是______。
(2)根据上图反应关系,写出下列B、F所含物质成分的化学式:B______;F_____。
(3)写出过程反应①的离子方程式_________________,固体B所含对应的金属其单质与磁性氧化铁在高温下反应的化学方程式__________________________。
(4)写出③中盐酸过量时的离子反应方程式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上曾经通过反应“3Fe + 4NaOH![]() Fe3O4 + 2H2↑+ 4Na↑”生产金属钠。下列说法正确的是
Fe3O4 + 2H2↑+ 4Na↑”生产金属钠。下列说法正确的是
A. 还原产物是钠Na和Fe3O4
B. 用磁铁可以将Fe与Fe3O4分离
C. 将生成的气体在空气中冷却可获得钠
D. 每生成1 mol H2,该反应转移的电子数约为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸性KMnO4、H2O2在生活、卫生医疗中常用作消毒剂,其中H2O2还可用于漂白,是化学实验室里必备的重要氧化试剂。高锰酸钾造成的污渍可用还原性的草酸(H2C2O4)去除,Fe(NO3)3也是重要的氧化试剂,下面是对这三种氧化剂性质的探究。
(1)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,写出该反应的离子方程式____________________,氧化产物与还原产物的物质的量之比为_______。
(2)取300 mL 0.2 mol·L-1的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则转移电子的物质的量是_____ mol。
(3)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的原因是_________________(用文字表达),又变为棕黄色的离子方程式是_____________________。
(4)测定KMnO4样品的纯度可用标准Na2S2O3溶液进行滴定,取0.474 g KMnO4样品溶解酸化后,用0.100 mol·L-1标准Na2S2O3溶液进行滴定,标准Na2S2O3溶液应盛装在___(填“酸式”或“碱式”)滴定管中。配平上述反应的离子方程式:___MnO4-+___S2O32-+____H+=____Mn2++_____SO42-+____H2O,实验中,滴定至终点时消耗Na2S2O3溶液12.00 mL,则该样品中KMnO4的物质的量是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将铁棒和石墨棒插入1 L 1 mol·L-1食盐水中。下列说法正确的是

A. 若电键K与N连接,铁被保护不会腐蚀
B. 若电键K与N连接,正极反应式是4OH--4e-===2H2O+O2↑
C. 若电键K与M连接,铁棒上有黄绿色气体产生
D. 若电键K与M连接,当两极共产生22.4 L(标准状况)气体时,生成了1 mol NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com