
【题目】在25.00 mL氢氧化钠溶液中逐滴加入0.2000 mol·L-1醋酸溶液,滴定曲线如图所示。
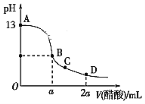
(1)写出氢氧化钠溶液与醋酸溶液反应的离子方程式___________。
(2)该氢氧化钠溶液的物质的量浓度为_________mol·L-1。
(3)设在B点时酸碱恰好中和,则a=____________。
(4)若所加入的酸为0.2000 mol·L-1的盐酸,则D点时溶液的c(H+)=________。
【答案】OH-+CH3COOH=CH3COO-+H2O 0.1000 12.50 0.05000 mol·L-1
【解析】
(1)氢氧化钠溶液与醋酸溶液反应,生成醋酸钠和水,其中书写离子方程式时,醋酸为弱电解质,不能拆成离子形式,据此书写离子方程式;
(2)由滴定曲线可知25.00 mL氢氧化钠溶液的pH=13,即c(OH-)=0.1mol/L,由此可得氢氧化钠溶液的浓度;
(3)在B点时酸碱恰好中和,n(H+)=n(OH-);
(4)若所加入的酸为0.2000 mol·L-1的盐酸,D点时加入盐酸的物质的量为0.2000 mol·L-1×2×0.0125L=0.005mol,此时加入NaOH的物质的量为0.1000mol/L×0.025L=0.0025mol,可知D点时加入的盐酸过量,且过量的盐酸的物质的量为0.005mol-0.0025mol=0.0025mol,根据过量的盐酸的物质的量,计算出D点时溶液的c(H+)。
(1)氢氧化钠溶液与醋酸溶液反应,生成醋酸钠和水,离子方程式为:OH-+CH3COOH=CH3COO-+H2O;
(2)由滴定曲线可知25.00 mL氢氧化钠溶液的pH=13,即c(OH-)=0.1000mol/L,由此可得氢氧化钠溶液的浓度为0.1000mol/L;
(3)在B点时酸碱恰好中和,n(H+)=n(OH-),即0.025L×c(OH-)=0.2000mol/L×a×10-3L,c(OH-)=0.1000mol/L,那么a=![]() =0.0125L=12.5mL;
=0.0125L=12.5mL;
(4)若所加入的酸为0.2000 mol·L-1的盐酸,D点时加入盐酸的物质的量为0.2000 mol·L-1×2×0.0125L=0.005mol,此时加入NaOH的物质的量为0.1000mol/L×0.025L=0.0025mol,可知D点时加入的盐酸过量,且过量的盐酸的物质的量为0.005mol-0.0025mol=0.0025mol,即D点时溶液中n(H+)=0.0025mol,此时c(H+)=![]() =
=![]() =0.05000 mol·L-1。
=0.05000 mol·L-1。


科目:高中化学 来源: 题型:
【题目】化合物H是一种有机材料中间体。实验室由芳香化合物A制备H的一种合成路线如下:
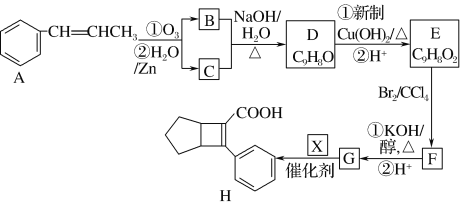
已知①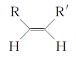
![]() RCHO+R′CHO
RCHO+R′CHO
②RCHO+R′CH2CHO![]()
![]() +H2O
+H2O
③![]()
请回答下列问题:
(1)芳香化合物B的名称为_______,C的同系物中相对分子质量最小的结构简式为_______。
(2)由F生成G的第①步反应类型为_______。
(3)X的结构简式为_______。
(4)写出D生成E的第①步反应的化学方程式________
(5)G与乙醇发生酯化反应生成化合物Y,Y有多种同分异构体,其中符合下列条件的同分异构体有____种,写出其中任意一种的结构简式________
①分子中含有苯环,且能与饱和碳酸氢钠溶液反应放出CO2;
②其核磁共振氢谱显示有4种不同化学环境的氢,且峰面积之比为6∶2∶1∶1。
(6)写出用![]() 为原料制备化合物
为原料制备化合物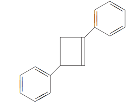 的合成线路,其他无机试剂任选________。
的合成线路,其他无机试剂任选________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利尿酸在奥运会上被禁用,其结构简式如下图所示。下列叙述正确的是( )

A. 利尿酸衍生物利尿酸甲酯的分子式是C14H14Cl2O4
B. 利尿酸分子内处于同一平面的原子不超过10个
C. 1 mol利尿酸能与7 mol H2发生加成反应
D. 利尿酸能与FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液电导率越大导电能力越强。常温下用0.100 mol·L-1盐酸分别滴定10.00 mL浓度均为0.100 mol·L-1的NaOH溶液和氨水溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是

A. 曲线①代表滴定氢氧化钠溶液的曲线
B. 滴定氨水的过程应该选择酚酞作为指示剂
C. b点溶液中:c(H+)>c(OH-)+c(NH4+)+c(NH3·H2O)
D. a、b、c、d四点的溶液中,水的电离程度最大的是c点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向100mL 0.01mol·L-1的NaHA溶液中分别加入浓度均为0.01mol·L-1的NaOH溶液和盐酸,混合溶液的pH随所加溶液体积的变化如图所示(忽略过程中的体积变化)。下列说法不正确的是
A. 25℃时,H2A的第二步电离平衡常数约为10-6
B. 水的电离程度:N>M>P
C. 随着盐酸的不断滴入,最终溶液的pH小于2
D. P点时溶液中存在:2c(H2A)+c(HA-)+c(H+)=c(OH-)+c(Na+)+c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电炉加热时用纯氧氧化管内样品,根据产物的质量确定有机物的组成,下列装置是用燃烧法确定有机物分子式常用的装置。
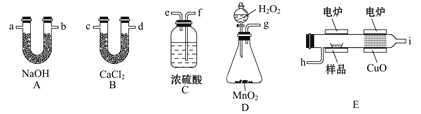
(1)产生的氧气按从左到右的流向,所选装置各导管的连接顺序是___________。
(2)C装置中浓H2SO4的作用是________。
(3)D装置中MnO2的作用是_____________。
(4)燃烧管中CuO的作用是______________。
(5)若准确称取0.90 g样品(只含C、H、O三种元素中的两种或三种),经充分燃烧后,A管质量增加1.32g,B管质量增加0.54 g,则该有机物的实验式为_______。
(6)要确立该有机物的分子式,还要知道___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用下图表示。下列关于海洋氮循环的说法正确的是
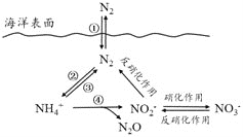
A. 海洋中的氮循环起始于氮的氧化
B. 海洋中的氮循环属于固氮作用的是③
C. 海洋中的反硝化作用一定有氧气的参与
D. 向海洋排放含NO3—的废水会影响海洋中NH4+的含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO是合成尿素、甲酸的原料。
(1)在100 kPa和T K下,由稳定单质生成1 mol化合物的焓变称为该物质在T K时的标准摩尔生成焓,用符号ΔHθ表示。已知石墨和一氧化碳的燃烧热分别为393.5 kJ·mol-1和283.0 kJ·mol-1,则CO(g)的ΔHθ=_________。
(2)合成尿素的反应:2NH3(g)+CO(g)CO(NH2)2(g)+H2(g) ΔH=-81.0 kJ·mol-1;T℃时,在体积为2 L 的恒容密闭容器中,将2 mol的NH3和1 mol CO混合反应,5 min时,NH3的转化率为80%。则0~5 min平均反应速率为v(CO)=_________。
已知:
温度/K | 398 | 498 | … |
平衡常数(K) | 126.5 | K1 | … |
则:K1________(填“>”或“<”)126.5;其判断理由是__________。
(3)若保持恒温恒容条件,将物质的量之和为3 mol的NH3和CO以不同的氨碳比进行反应,结果如图所示:
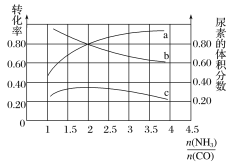
①若图中c表示平衡体系中尿素的体积分数,则a表示________的转化率。
②当![]() =________时,尿素含量最大;在该条件下,对于该反应既能增大反应速率又能使平衡正向移动的措施是_____(写一种)。
=________时,尿素含量最大;在该条件下,对于该反应既能增大反应速率又能使平衡正向移动的措施是_____(写一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据所给条件推出的结论不正确的是( )
选项 | 条件 | 结论 |
A | 在水溶液中或熔融状态下可以导电的化合物称为电解质 | CH3COOH水溶液中存在:CH3COOH |
B | 凡是能给出质子的分子或离子称为酸,凡是能接受质子的分子或离子称为碱 | H2O既是酸又是碱 |
C | Fe3Cl8可以改写为FeCl2·2FeC13 | Fe3I8可以改写为FeI·2FeI3 |
D | HCl在一定条件下能被MnO2氧化为Cl2 | HBr在一定条件下也能被MnO2氧化为Br2 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com