
【题目】下列各组离子,在指定的环境中一定能大量共存的是( )
A.常温下,在c(H+)/c(OH﹣)=1×1012的溶液中:I﹣、Cl﹣、NO ![]() 、Na+
、Na+
B.在能使石蕊变红色的溶液中:Na+、S2﹣、SO ![]() 、CO
、CO ![]()
C.在加入铝粉能产生H2的溶液中:NH ![]() 、Na+、NO
、Na+、NO ![]() 、Cl﹣
、Cl﹣
D.常温下由水电离出的c(H+)=1×10﹣12 mol?L﹣1的溶液中:K+、Cl﹣、NO ![]() 、Na+
、Na+
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】在使用分液漏斗进行分液时,正确的操作是( )
A. 上层液体经漏斗下口放出
B. 分离液体时,将漏斗拿在手上进行分离
C. 分离液体时,使分液漏斗口上的小孔与大气相通,打开活塞
D. 分液漏斗中盛装的是液体,振荡后不必扭开活塞把气体放出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各组离子中,能大量共存的( )
A.Ag+、NO3﹣、Na+、Cl﹣
B.K+、HCO3﹣、Cl﹣、Al3+
C.NO3﹣、Fe2+、H+、Br﹣
D.K+、Cl﹣、SO42﹣、NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氧化铝和氢氧化铝的说法正确的是( )
A. 氧化铝是一种比较好的耐火材料,可用来制造耐火坩埚
B. 氧化铝是典型的两性氧化物,可与氨水反应生成四羟基合铝酸盐
C. 因为氢氧化铝受热易分解,所以具有两性
D. 两性氢氧化物只能与强酸、强碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式错误的是( )
A.NaHCO3═Na++H++CO ![]()
B.NaHSO4(溶液)═Na++H++SO ![]()
C.MgCl2═Mg2++2Cl﹣
D.Ba(OH)2═Ba2++2OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应A2+3B2=2C来说,以下表示中,反应速率最快的是( )
A.v(B2)=0.8 mol/(Ls)
B.v(A2)=0.5 mol/(Ls)
C.v(C)=0.9 mol/(Ls)
D.v(B2)=1.2 mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中甲曲线表示在最适温度下,某种酶促反应速率与反应物浓度之间的关系。其余两条曲线分别表示该酶促反应的反应速率受温度和pH的影响情况。回答下列问题:

(1)甲曲线中,若在A点适当提高温度,反应速率将会_____________________;在B点适当增加酶的浓度,反应速率将会__________________。
(2)丙曲线中,H点代表该酶的_____________________。
(3)若想要短期保存该酶,应选择曲线中的________点所对应的温度。
(4)探究温度对酶活性的影响时,通常选择_________________________(填“淀粉酶”或“过氧化氢酶”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一学生设计了如下实验方法分离NaCl和CaCl2两种固体混合物 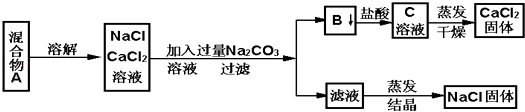 填空和回答下列问题
填空和回答下列问题
(1)B物质是(写化学式)
(2)按此实验方案分离得到的NaCl,经分析含有杂质,是因为上述方案中某一步设计有毛病,这一步的正确设计方案应是 .
(3)若要测定该样品中NaCl和CaCl2的质量比,可称量干燥的B物质和另一物质的质量,这种物质是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在银锌原电池中,以硫酸铜为电解质溶液,锌为极,电极上发生的是反应(“氧化”或“还原”),电极反应式为 , 锌片上观察到的现象为;银电极上的电极反应式是 , 银片上观察到的现象是 . 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com