
ĻĀĮŠ·“Ó¦¼ČŹōÓŚŃõ»Æ»¹Ō·“Ó¦£¬ÓÖŹōÓŚĪüČČ·“Ó¦µÄŹĒ
A£®ĀĮʬŗĶĻ”ŃĪĖį·“Ó¦ B£®Ba(OH)2”¤8H2OÓėNH4ClµÄ·“Ó¦
C£®¼×ĶéŌŚŃõĘųÖŠµÄČ¼ÉÕ D£®×ĘČȵÄĢ¼Óė¶žŃõ»ÆĢ¼µÄ·“Ó¦
 æŚĖ抔דŌŖæŚĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
æŚĖ抔דŌŖæŚĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
·Ö×ÓŹ½ĪŖC7H16µÄĶéĢžÖŠ£¬ŗ¬ÓŠ3øö¼×»łµÄĶ¬·ÖŅģ¹¹ĢåŹżÄæŹĒ ( )
A£®2ÖÖ B£®3ÖÖ C£®4ÖÖ D£®5ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅųÖŹĘ÷ĆóČÕ¾Ć±ķĆę»įÖš½„±äŗŚ£¬ÕāŹĒÉś³ÉĮĖAg2SµÄŌµ¹Ź£¬øł¾Żµē»ÆѧŌĄķæɽųŠŠČēĻĀ“¦Ąķ£¬ŌŚĀĮÖŹČŻĘ÷ÖŠ¼ÓČėŹ³ŃĪČÜŅŗ£¬ŌŁ½«±äŗŚµÄŅųĘ÷½žČėøĆČÜŅŗÖŠ£¬Ņ»¶ĪŹ±¼äŗó·¢ĻÖŗŚÉ«»įĶŹČ„£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ (””””)
A£®“¦Ąķ¹ż³ĢÖŠŅųĘ÷Ņ»Ö±±£³ÖŗćÖŲ
B£®ŅųĘ÷ĪŖÕż¼«£¬Ag2S±»»¹ŌÉś³Éµ„ÖŹŅų
C£®øĆ¹ż³ĢÖŠ×Ü·“Ó¦ĪŖ2Al£«3Ag2S===6Ag£«Al2S3
D£®ŗŚÉ«ĶŹČ„µÄŌŅņŹĒŗŚÉ«Ag2S×Ŗ»ÆĪŖ°×É«AgCl
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ģ«ŃōÄܹā·ü·¢µēĻµĶ³ŹĒ±»³ĘĪŖ”°21ŹĄ¼ĶĀĢÉ«¹āŌ“”±µÄ°ėµ¼ĢåÕÕĆ÷(LED)ĻµĶ³(ČēĶ¼)”£ŅŃÖŖ·¢³ö°×¹āµÄLEDŹĒ½«GaNŠ¾Ę¬ŗĶīĘĀĮŹÆĮńŹÆ(YAG£¬»ÆѧŹ½£ŗY3Al5O12)Š¾Ę¬·ā×°ŌŚŅ»Ęš×ö³É”£ĻĀĮŠĖµ·ØÖŠ²»ÕżČ·µÄŹĒ (””””)

A£®¹ā·ü·¢µēŹĒ½«Ģ«ŃōÄÜ×Ŗ±äĪŖµēÄÜ
B£®ÉĻĶ¼ÖŠNĒų°ėµ¼ĢåĪŖøŗ¼«£¬PĒų°ėµ¼ĢåĪŖÕż¼«£¬µēĮ÷“ÓaĮ÷Ļņb
C£®YAGÖŠīĘĻŌ£«3¼Ū
D£®GaÓėNŌŚŌŖĖŲÖÜĘŚ±ķÖŠ²»“¦ÓŚĶ¬Ņ»Ö÷×å
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Č«·°ŅŗĮ÷µē³ŲŹĒŅ»ÖÖ»īŠŌĪļÖŹ³ŹŃ»·Į÷¶ÆŅŗĢ¬µÄµē³Ų£¬ÄæĒ°·°µē³Ų¼¼ŹõŅŃ¾Ē÷½ü³ÉŹģ”£ĻĀĶ¼ŹĒ·°µē³Ų»ł±¾¹¤×÷ŌĄķŹ¾ŅāĶ¼£ŗ

Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)ĮņĖįŌŚµē³Ų¼¼ŹõŗĶŹµŃéŹŅÖŠ¾ßÓŠ¹ć·ŗµÄÓ¦ÓĆ£¬ŌŚ“«Ķ³µÄĶŠæŌµē³ŲÖŠ£¬ĮņĖįŹĒ_________£¬ŹµŃéŹŅÖŠÅäÖĘĮņĖįŃĒĢśŹ±ŠčŅŖ¼ÓČėÉŁĮæĮņĖį£¬ĮņĖįµÄ×÷ÓĆŹĒ__________”£
(2)·°µē³ŲŹĒŅŌČܽāÓŚŅ»¶ØÅضČĮņĖįČÜŅŗÖŠµÄ²»Ķ¬¼ŪĢ¬µÄ·°Ąė×Ó(V2£«”¢V3£«”¢VO2£«”¢VO )ĪŖÕż¼«ŗĶøŗ¼«µē¼«·“Ó¦µÄ»īŠŌĪļÖŹ£¬µē³Ų×Ü·“Ó¦ĪŖVO2£«£«V3£«£«H2O
)ĪŖÕż¼«ŗĶøŗ¼«µē¼«·“Ó¦µÄ»īŠŌĪļÖŹ£¬µē³Ų×Ü·“Ó¦ĪŖVO2£«£«V3£«£«H2O V2£«£«VO
V2£«£«VO £«2H£«”£·ÅµēŹ±µÄÕż¼«·“Ó¦Ź½ĪŖ____________________________________________£¬
£«2H£«”£·ÅµēŹ±µÄÕż¼«·“Ó¦Ź½ĪŖ____________________________________________£¬
³äµēŹ±µÄŅõ¼«·“Ó¦Ź½ĪŖ_________________________________________________”£
·Åµē¹ż³ĢÖŠ£¬µē½āŅŗµÄpH________(Ģī”°Éżøß”±”¢”°½µµĶ”±»ņ”°²»±ä”±)”£
(3)·°µē³Ų»ł±¾¹¤×÷ŌĄķŹ¾ŅāĶ¼ÖŠ”°Õż¼«µē½āŅŗ”±æÉÄÜŹĒ________(Ģī×ÖÄøŠņŗÅ)”£
a£®VO ”¢VO2£«»ģŗĻŅŗ b£®V3£«”¢V2£«»ģŗĻŅŗ
”¢VO2£«»ģŗĻŅŗ b£®V3£«”¢V2£«»ģŗĻŅŗ
c£®VO ČÜŅŗ d£®VO2£«ČÜŅŗ
ČÜŅŗ d£®VO2£«ČÜŅŗ
e£®V3£«ČÜŅŗ f£®V2£«ČÜŅŗ
(4)Äܹ»Ķعż·°µē³Ų»ł±¾¹¤×÷ŌĄķŹ¾ŅāĶ¼ÖŠ”°øōĤ”±µÄĄė×ÓŹĒ______________________
__________________________________________________ӣ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆĢśĘ¬Óė10mL0.1mol”¤L£1ĮņĖį·“Ó¦ÖĘČ”ĒāĘųŹ±£¬ĻĀĮŠ“ėŹ©ÖŠ²»ÄÜŹ¹ĒāĘųÉś³ÉĖŁĀŹ¼ÓæģµÄŹĒ
A£®¼ÓČČ B£®¼ÓČė10mL0.1mol”¤L£1ĮņĖį
C£®µĪ¼ÓÉŁĮæCuSO4ČÜ Ņŗ D£®²»ÓĆĢśĘ¬£¬øÄÓĆĢś·Ū
Ņŗ D£®²»ÓĆĢśĘ¬£¬øÄÓĆĢś·Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| C | ||
| B | ||
| D | E |
ĘäÖŠA”¢B”¢C”¢D”¢EĪåÖÖŌŖĖŲŌŚÖÜĘŚ±ķÖŠĖł“¦µÄĻą¶ŌĪ»ÖĆ
ČēÓŅĶ¼ĖłŹ¾£¬ĘäÖŠA”¢B”¢CĪ»ÓŚ¶ĢÖÜĘŚ”£ÓÖÖŖA”¢CĮ½ŌŖĖŲµÄŌ×Ó
ŗĖĶāµē×ÓŹżÖ®ŗĶµČÓŚBŌ×ÓµÄÖŹ×ÓŹż£¬BŌ×ÓŗĖÄŚÖŹ×ÓŹżŗĖÖŠ×ÓŹżĻąµČ”£
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©A”¢B”¢C”¢£ÅČżÖÖŌŖĖŲµÄĆū³Ę·Ö±šĪŖ£ŗ__________”¢__________”¢__________”¢”””””””””””£
£Ø£²£©ÓėCŌŖĖŲĪ»ÓŚĶ¬Ņ»Ö÷×åµÄĮķŅ»ÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬ĘäŌŖĖŲ·ūŗÅŹĒ £¬Ęä×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ»ÆѧŹ½ĪŖ£ŗ”””””””””””””””£
£Ø£³£©CŌŖĖŲµÄµ„ÖŹÓėH2·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ ”£
£Ø£“£©EµÄŌŖĖŲ·ūŗÅŹĒ £»DµÄŌ×ÓŠņŹżĪŖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
³£ĪĀŹ±£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A£® pH£½9µÄNH4ClÓėNH3?H2O»ģŗĻČÜŅŗÖŠc(Cl-)>c(NH4+)
B£® pH£½2.5µÄæÉĄÖÖŠc(H£«) ŹĒpH£½3.5µÄÄūĆŹĖ®ÖŠc(H£«)µÄ10±¶
C£® AgClŌŚ0.1mol /L CaCl2ČÜŅŗŗĶ0.1mol/L NaClČÜŅŗÖŠµÄČܽā¶ČĻąĶ¬
D£® 1 mL 1mol /L Na2CO3ČÜŅŗ¼ÓĖ®Ļ”ŹĶÖĮ100mL£¬ pHŗĶKw¾ł¼õŠ”
| |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
(1)±ź³öÓŠ»śĪļ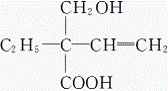 ÖŠµÄŹÖŠŌĢ¼Ō×Ó
ÖŠµÄŹÖŠŌĢ¼Ō×Ó
(2)Š“³ö“ĖÓŠ»śĪļ·Ö±š·¢ÉśĻĀĮŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½”£
¢ŁÓėH2¼Ó³É _____ ______ _______ __
¢ŚÓėŅŅĖį·“Ó¦_____ ______ _______ __
¢ŪÓėNa·“Ó¦_____ _______ _______ __
£Ø3£©µŚ_____ __·“Ó¦ŗó£¬Éś³ÉµÄÓŠ»śĪļ·Ö×Ó²»ŌŁŗ¬ÓŠŹÖŠŌĢ¼Ō×Ó.
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com