
| A�������ڿ����г��ֺ�ɫ�����⣬�为����ӦʽΪ��Fe-3e-�TFe3+ |
| B��������þ��ɫ���������Ȼ����Һ��Mg��OH��2+2NH4+�TMg2++2NH3?H2O |
| C����������Һ�еμ�����������Һ��SO42-��ȫ������Al3++2SO42-+2Ba2++4OH-�T2BaSO4��+2AlO2-+2H2O |
| D��Ư����Һ�м��Ȼ�����Һ�����������ɫ������Fe3++3ClO-+3H2O�TFe��OH��3��+3HClO |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��C5H9NO |
| B��C5H9NO2 |
| C��C5H9NO3 |
| D��C5H9NO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.05 g/mol |
| B��0.05 mol |
| C��32 g |
| D��32 g/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ʯӢ��������������Һ��SiO2+2OH-�TSiO32-+H2O |
| B��������Ͷ������������Һ�У�2Al+2OH-�T2AlO2-+H2�� |
| C����������������Һ��Ӧ��Fe+Fe3+�T2Fe2+ |
| D����������ˮ��Ӧ��Na+2H2O�TNa++2OH-+H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������Na2CO3 |
| B���ᡡ���ᡡH2S |
| C������������ɱ���CO2 |
| D���Ρ�̼李���NH4��2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A����ϩˮ����CH2=CH2+H2O
| |||
B�������Ƿ��ͣ�C6H12O6
| |||
C��������ˮ�⣺CH3CH2Br+H2O
| |||
D����������ˮ�⣺CH3CH2COOCH2CH3+H2O
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
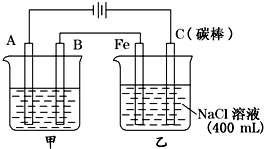 ��ͼΪ������ļ���������
��ͼΪ������ļ���������| ���� | Fe��OH��2 | Fe��OH��3 | Zn��OH��2 | Cu��OH��2 |
| KSP | 8.0��10-16 | 4.0��10-38 | 3.0��10-17 | 2.2��10-20 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com