
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L的正戊烷完全燃烧需要氧气分子数为4NA | |
| B. | 标准状况下,22.4L乙烷中所含电子对数目为6NA | |
| C. | 26g乙炔和苯的混合物,含有原子总数为4NA | |
| D. | 标准状况下,22.4L甲烷与氯气光照取代发生一氯取代,需要氯气0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
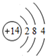 ,D在元素周期表中的位置第3周期第VIA族
,D在元素周期表中的位置第3周期第VIA族 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
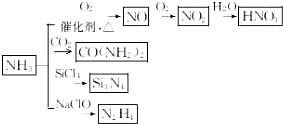
| A. | 图中所述反应都发球氧化还原反应 | |
| B. | CO(NH2)2与氰酸铵(NH4CNO)互为同素异形体 | |
| C. | Si3N4属于离子化合物 | |
| D. | NH3与NaClO反应,N2N4是氧化产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 清晨在密林中看到一缕缕光束 | |
| B. | 盐酸与硝酸银溶液反应生成白色沉淀 | |
| C. | 豆浆中加入盐卤做豆腐 | |
| D. | 一束平行光射入蛋白质溶液中,侧面可看到一束光亮的通路 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性比较:S2O82 ->MnO4- | |
| B. | 氧化剂S2O82-的摩尔质量为 192 g/mol | |
| C. | 该反应中酸性介质可以为盐酸 | |
| D. | 若有0.1 mol氧化产物生成,则转移电子 0.5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若要除去CO2中含有的少量SO2气体,可通过盛有饱和NaHCO3溶液的洗气瓶 | |
| B. | 在实验室中使用金属钠时若不慎着火,可立即用细沙灭火 | |
| C. | 用带有玻璃塞的玻璃瓶盛放NaOH溶液 | |
| D. | 测溶液pH时,可用干净的玻璃棒蘸取溶液滴到放在表面皿上的pH试纸上 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com