
Ⅰ.某实验A小组设计生产亚氯酸钠(NaClO2)的主要流程如图,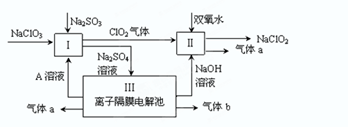
已知NaClO2是一种强氧化性漂白剂,广泛用于纺织、印染工业。它在碱性环境中稳定存在。
(1)双氧水的电子式为 ,装置Ⅰ中发生反应的还原剂是 (填化学式)。
(2)A的化学式是 ,装置Ⅲ电解池中A在 极区产生,若装置Ⅲ中生成气体a为 11.2 L(标准状况),则理论上通过电解池的电量为 (已知法拉第常数F="9.65×l" 04C· mol-1)。
(3)装置Ⅱ中反应的离子方程式是 。
Ⅱ.某实验B小组测定金属锡合金样品的纯度(仅含少量锌和铜,组成均匀),将样品溶于足量盐酸: Sn+ 2HCl=SnCl2+H2↑,过滤,洗涤。将滤液和洗涤液合并再加过量的FeCl3溶液。最后可用一定浓度的K2Cr2O7酸性溶液滴定生成的Fe2+,此时还原产物为Cr3+。现有锡合金试样1.23g,经上述反应、操作后,共用去0.200mol/L的K2Cr2O7的酸性溶液15.00mL。
(4) 列式计算样品中锡的质量分数。
(5)用上述样品模拟工业上电解精炼锡,如图: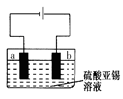
b极发生电极反应式 ,当得到11.90g纯锡时,电解质溶液质量减轻0.54g,则锡合金质量减少_______ g(结果保留一位小数)。
(1) Na2SO3
Na2SO3
(2)H2SO4 阳 1.93×l 05C (3)2ClO2 + H2O2 + 2OH-= 2ClO2-+ O2↑+ 2H2O
(4)87.1%
由关系式6Fe2+ ~ 3Sn2+ ~ Cr2O72– 得出n(Sn)="0.009" mol
∴ W%=
(5)Sn -2e-=Sn2+ Zn-2e-=Zn2+ 12.3g
解析试题分析:(1)在双氧水分子中每个O原子与一个H原子形成共用电子对,再与另一个O原子形成共用电子对。所以它的电子式为 。在装置Ⅰ中发生反应NaClO3把Na2SO3氧化为Na2SO4,它本身被还原为ClO2.所以还原剂是Na2SO3。(2)在装置Ⅱ中中发生反应:ClO2+H2O2+NaOH=NaClO2+H2O+O2↑.Na2SO4溶液在装置Ⅲ电解池发生氧化还原反应:溶液中的阳离子的氧化性:H+>Na+,所以在阴极发生反应:2H++2e-=H2↑.由于破坏了附近的水的电离平衡,最终导致该区域的溶液显碱性,分离出NaOH溶液。溶液中的阴离子的还原性:OH->SO42-,所以在阳极发生反应为:4OH—+4e-=O2↑+2H2O。消耗了水电离产生的OH-,破坏了水的电离平衡,水继续电离。最终导致该区域的溶液显酸性。因此该阳极区产生的是氧气产物A为硫酸。化学式是H2SO4。n(O2)=" 11.2L÷" 22.4L/mol =0.5mol.则n(e-)=4×0.5mol=2mol.则理论上通过电解池的电量为2mol×9.65×l 04C/ mol=" 1.93×l" 05C.(3)装置Ⅱ中反应的化学方程式为ClO2+ H2O2+NaOH=NaClO2+H2O+O2↑的离子方程式是2ClO2 + H2O2 + 2OH-= 2ClO2-+ O2↑+ 2H2O。(4)在反应过程中发生的反应为Sn2++ 2Fe3+= Sn4++ 2Fe2+, 6Fe2++Cr2O72- +14H+= 6Fe3++2Cr3++ 7H2O 。由方程式得关系式为:6Fe2+ ~ 3Sn2+ ~ Cr2O72–。n(Cr2O72-)= 0.200mol/L× 0.01500L=0.003mol.,所以n(Sn)="0.009" mol.m(Sn)=" 0.009" mol×119g/mol=1.071g.所以样品中锡的质量分数W%=
。在装置Ⅰ中发生反应NaClO3把Na2SO3氧化为Na2SO4,它本身被还原为ClO2.所以还原剂是Na2SO3。(2)在装置Ⅱ中中发生反应:ClO2+H2O2+NaOH=NaClO2+H2O+O2↑.Na2SO4溶液在装置Ⅲ电解池发生氧化还原反应:溶液中的阳离子的氧化性:H+>Na+,所以在阴极发生反应:2H++2e-=H2↑.由于破坏了附近的水的电离平衡,最终导致该区域的溶液显碱性,分离出NaOH溶液。溶液中的阴离子的还原性:OH->SO42-,所以在阳极发生反应为:4OH—+4e-=O2↑+2H2O。消耗了水电离产生的OH-,破坏了水的电离平衡,水继续电离。最终导致该区域的溶液显酸性。因此该阳极区产生的是氧气产物A为硫酸。化学式是H2SO4。n(O2)=" 11.2L÷" 22.4L/mol =0.5mol.则n(e-)=4×0.5mol=2mol.则理论上通过电解池的电量为2mol×9.65×l 04C/ mol=" 1.93×l" 05C.(3)装置Ⅱ中反应的化学方程式为ClO2+ H2O2+NaOH=NaClO2+H2O+O2↑的离子方程式是2ClO2 + H2O2 + 2OH-= 2ClO2-+ O2↑+ 2H2O。(4)在反应过程中发生的反应为Sn2++ 2Fe3+= Sn4++ 2Fe2+, 6Fe2++Cr2O72- +14H+= 6Fe3++2Cr3++ 7H2O 。由方程式得关系式为:6Fe2+ ~ 3Sn2+ ~ Cr2O72–。n(Cr2O72-)= 0.200mol/L× 0.01500L=0.003mol.,所以n(Sn)="0.009" mol.m(Sn)=" 0.009" mol×119g/mol=1.071g.所以样品中锡的质量分数W%= 。(5)电解精炼Sn时,用粗Sn作阳极,精Sn作阴极。含Sn2+离子的溶液作电解质溶液。所以b极为阳极。阳极电极反应式Sn -2e-=Sn2+;Zn-2e-=Zn2+。阴极电极反应式为:Sn2++2e-=Sn。即相当于一部分的Sn是Zn发生置换反应Zn+Sn2+=Zn2++Sn。阳极每有65gZn反应,阴极生成Sn119g,溶液减轻54g.现在溶液减轻0.54g,则发生反应的Zn为0.01mol,其质量为0.65g,由该Zn置换出来的Sn为0.01mol。其质量为1.19g.所以参加反应的锡质量为11.90-1.19= 10.71g,因为Sn的含量为87.1%,所以Sn合金的质量为10.71g÷87.1%=12.3g.
。(5)电解精炼Sn时,用粗Sn作阳极,精Sn作阴极。含Sn2+离子的溶液作电解质溶液。所以b极为阳极。阳极电极反应式Sn -2e-=Sn2+;Zn-2e-=Zn2+。阴极电极反应式为:Sn2++2e-=Sn。即相当于一部分的Sn是Zn发生置换反应Zn+Sn2+=Zn2++Sn。阳极每有65gZn反应,阴极生成Sn119g,溶液减轻54g.现在溶液减轻0.54g,则发生反应的Zn为0.01mol,其质量为0.65g,由该Zn置换出来的Sn为0.01mol。其质量为1.19g.所以参加反应的锡质量为11.90-1.19= 10.71g,因为Sn的含量为87.1%,所以Sn合金的质量为10.71g÷87.1%=12.3g.
考点:考查电子式、离子方程式、氧化剂、还原剂的判断、电解原理及物质纯度的计算的知识。


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:填空题
已知:氧化性:KMnO4>HNO3;Bi位于周期表中ⅤA族,+3价较稳定,Bi2O3为碱性氧化物,Bi3+的溶液为无色。取一定量硝酸酸化的Mn(NO3)2溶液依次进行下列实验,现象记录如下:
①向其中加入适量的NaBiO3,溶液变为紫红色。②继续滴加适量H2O2,紫红色褪去,并有气泡产生。③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
回答下列问题:
(1)写出实验①反应的离子方程式: 。
(2)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为 。
(3)向反应③得到的溶液中通入SO2气体,看到的现象是 。
(4)若实验②放出了336 mL气体(标准状况),则反应①被氧化的Mn(NO3)2为 mol。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4二主要流程如下: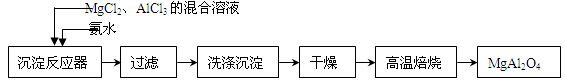
⑴制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式 。
⑵如图所示,过滤操作中的一处错误是 。判断流程中沉淀是否洗净所用的试剂是 。高温焙烧时,用于盛放固体的仪器名称是 。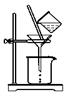
⑶在25℃下,向浓度均为0.01 mol?L-1的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成_______沉淀(填化学式),生成该沉淀的离子方程式_______ ______________
(已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3×10 -34。)
⑷无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。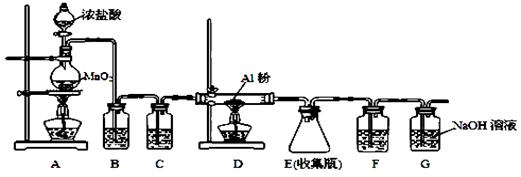
装置B中盛放饱和NaCl溶液,该装置的主要作用是 ; F中试剂的作用是 ;用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为 。
⑸将Mg、Cu组成的3.92g混合物投入过量稀硝酸中,充分反应后,固体完全溶解时收集到还原产物NO气体1.792L(标准状况),向反应后的溶液中加入4mol/L的NaOH溶液80mL时金属离子恰好完全沉淀。则形成沉淀的质量为 g。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
I. 今有H2、Cl2混合气100 mL(标况),其中一种气体的体积为45mL。光照使两种气体发生反应后恢复到标况,气体体积为 mL。为了说明反应后气体中H2或Cl2有剩余,使气体通过10 mL水,并使剩余气体干燥后恢复到标况,
(1)若仍剩余___mL,证明有___剩余,理由是_____;
(2)若溶液有___性质,证明有___剩余,理由是________________________。
II.一位同学设计了一套用浓盐酸和KMnO4固体制取少量氯气并比较氯气与碘单质的氧化性强弱的微型装置(如图所示)。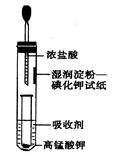
(1)下列溶液能吸收Cl2的是________。
| A.饱和食盐水 | B.Na2SO4溶液 |
| C.NaOH溶液 | D.浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
金属冶炼与处理常涉及氧化还原反应。
(1)由下列物质冶炼相应金属时采用电解法的是________。
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)辉铜矿(Cu2S)可发生反应:2Cu2S+2H2SO4+5O2=4CuSO4+2H2O,该反应的还原剂是________。当1 mol O2发生反应时,还原剂所失电子的物质的量为________mol。向CuSO4溶液中加入镁条时有气体生成,该气体是________。
(3)如图为电解精炼银的示意图,________(填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色气体产生,则生成该气体的电极反应式为__________________________。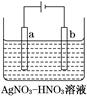
(4)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用是______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
高铁酸钾(K2FeO4)具有很强的氧化性,在生产、生活中有广泛应用。
(1)K2FeO4常用做高效水处理剂,其两种作用分别是_____。
[已知:FeO42-+3e-+4H2O Fe(OH)3+5OH-]
Fe(OH)3+5OH-]
(2)制备K2FeO4可以采用湿式氧化法,流程如下图: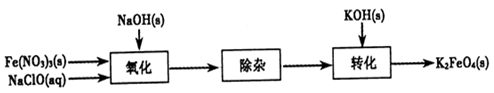
①完成氧化工序的离子方程式:
②除杂工序目的是除去Na2FeO4溶液中的杂质,除去的杂质主要有_____(写化学式)。
③转化工序控制在某温度下进行,则该温度下溶解度:Na2FeO4_____K2FeO4 (填“>”、“<”或“=”)。
(3)实验室模拟工业电解法制取K2FeO4,装置如右图。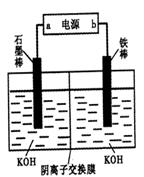
①此装置中电源的负极是____(填“a”或“b”)。
②阳极的电极反应式为______。
(4)已知K2FeO4稀溶液中存在如下平衡:4FeO42-+10H2O 4Fe(OH)3+8OH-+3O2。实验测得K2FeO4溶液浓度与温度和pH的关系分别如下图所示:
4Fe(OH)3+8OH-+3O2。实验测得K2FeO4溶液浓度与温度和pH的关系分别如下图所示: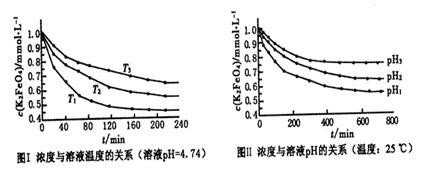
①由图I可得出的结论:该反应的△H___0(填“>”、“<”或“=”)。
②图Ⅱ中pH1___pH3(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业上以碳酸锰矿为主要原料生产MnO2的工艺流程如下: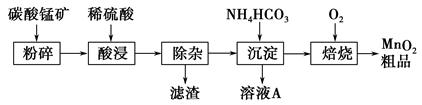
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Pb(OH)2 | Mn(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 | 8.0 | 8.3 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 | 8.8 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业上利用含有一定浓度的I2和CuSO4溶液的工业废水制备饲料添加剂Ca(IO3)2,其生产流程如下: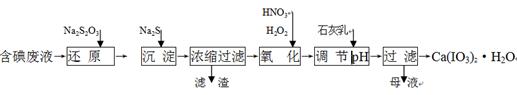
已知:Ca(IO3)2微溶于水,溶于硝酸;Ksp(CuI)=1.1×10-12, Ksp(Cu2S)=2.5×10-48;
氧化性: HNO3>IO3—>H2O2
(1)“还原”过程中主要反应的化学方程式为:2Na2S2O3+I2 = + 2NaI。
(2)在还原过程还伴随有CuI生成,写出加入Na2S的离子反应方程式 。
(3)在氧化过程中先加入H2O2再加入浓硝酸,而不直接加入浓硝酸的目的是 。
(4)加入的石灰乳在溶液中反应而得到Ca(IO3)2,则要调节pH至 (填“酸性” 或“中性”或“碱性”),原因是 。
(5)Ca(IO3)2也可用电化学氧化法制取:先充分电解KI溶液,然后在电解后的溶液中加入CaCl2,最后过滤得到Ca(IO3)2。写出电解时阳极发生的电极反应方程式 ,用该方法制取Ca(IO3)2,每1kg碘化钾理论上可生产纯度为97.8%Ca(IO3)2的质量为 ____kg(计算结果保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
许多物质的氧化能力受溶液酸碱性的影响。高锰酸钾在不同的条件下发生的还原反应如下:
MnO4—+ 5e + 8H+ → Mn2+ + 4H2O
MnO4— + 3e + 2H2O → MnO2 + 4OH—
MnO4— + e → MnO42—(溶液呈绿色)
MnO2的还原反应可表示如下:MnO2+4H+ + 2e → Mn2++2H2O
(1)MnO2与稀盐酸不能制取氯气,其原因是 。
(2)将SO2通入KMnO4溶液中,发生还原反应的过程为______→_______
(用化学式或离子符号表示)。
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色。下列叙述正确的是________(选填编号)。
a.氧化性:PbO2>KMnO4 b.还原性:PbO2> KMnO4
c.该反应可以用盐酸酸化
(4)将高锰酸钾溶液逐滴加入到硫化钾溶液中可发生如下反应,其中K2SO4和S的物质的量之比为3:2。完成并配平该反应的化学方程式。
___KMnO4+___K2S+___ _____ → ___K2MnO4 +___K2SO4 +__S↓+___ ___
反应若生成5.44 g单质硫,反应过程中转移电子的物质的量为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com