
| A. | 用核磁共振氢谱不能鉴别1-丙醇和2-丙醇 | |
| B. | 实验证实 可使Br2的CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 可使Br2的CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 | |
| C. | 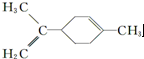 所有碳原子一定在同一平面上 所有碳原子一定在同一平面上 | |
| D. | 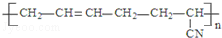 的单体是CH3-C≡C-CH3和CH2═CH-CN 的单体是CH3-C≡C-CH3和CH2═CH-CN |
分析 A.根据1-丙醇中含有4种不同环境的氢原子,2-丙醇含有3种不同环境的氢原子;
B.根据碳碳双键能与单质溴发生加成反应使Br2的CCl4溶液褪色;
C.根据碳环中碳原子不在同一平面上;
D.当高聚物中出现双键时,应考虑单体中含三键或是二烯;
解答 解:A.1-丙醇中含有4种不同环境的氢原子,2-丙醇含有3种不同环境的氢原子,故可用核磁共振氢谱鉴别1-丙醇和2-丙醇,故A错误;
B. 可使Br2的CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键,故B正确;
可使Br2的CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键,故B正确;
C.碳环中碳原子不在同一平面上,所以 所有碳原子不在同一平面上,故C错误;
所有碳原子不在同一平面上,故C错误;
D.该高聚物链节主链不含杂原子,属于加聚反应生成的高聚物,链节主链上存在碳碳双键结构,有6个碳原子,其单体必为两种,按如图所示断开 ,在将双键中的1个C-C打开,然后将半键闭合即可的该高聚物单体为:CH2=CH-CH=CH2、CH2=CH-CN,故D错误.
,在将双键中的1个C-C打开,然后将半键闭合即可的该高聚物单体为:CH2=CH-CH=CH2、CH2=CH-CN,故D错误.
故选B.
点评 本题考查物质的结构与性质,涉及氢原子的种类、原子共面、碳碳双键的性质以及高聚物的单体等,难度不大.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:选择题
| A. | 该反应为吸热反应 | B. | CO2分子由极性键形成的极性分子 | ||
| C. | HCHO分子中有3个σ键,1个π键 | D. | 每生成1.8gH2O消耗2.24L O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.2 | B. | 2.4 | ||
| C. | 0 | D. | 缺少条件,无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在过氧化钠与水的反应中.固体每增重mg,转移电子为0.2NA | |
| B. | 在准状况下,2.24LCl2与过量NaOH溶液反应,转移的电子总数为0.2NA | |
| C. | 已知反应:2NH3+NO+NO2═2N2+3H2O,每生成2molN2转移的电子数为6NA | |
| D. | 标准状况下,22.4LCCl4中含有的碳原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
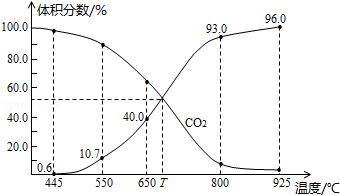
| A. | 550℃时,若充入惰性气体,v正,v逆均减小 | |
| B. | 650℃时,反应达平衡后CO2的转化率为25.0% | |
| C. | T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动 | |
| D. | 925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=23.04P总 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
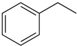 (g)→
(g)→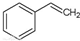 (g)+H2(g),△H=+117.6kJ/mol;
(g)+H2(g),△H=+117.6kJ/mol; +CO(g)+H2O(g) △H=+158.8 kJ/mol
+CO(g)+H2O(g) △H=+158.8 kJ/mol
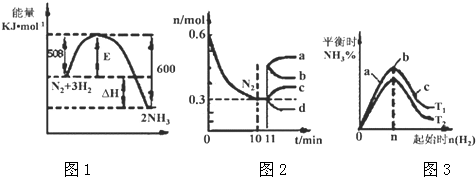
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com