
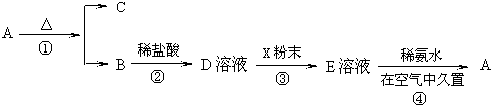
分析 E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色,则A为Fe(OH)3,由转化关系可知,A加热分解生成B为Fe2O3,C为H2O,D为FeCl3,X为Fe,E为FeCl2.
解答 解:E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色,则A为Fe(OH)3,由转化关系可知,A加热分解生成B为Fe2O3,C为H2O,D为FeCl3,X为Fe,E为FeCl2.
(1)物质A是Fe(OH)3,故答案为:Fe(OH)3;
(2)反应②的离子反应方程式为:Fe2O3+6H+=2 Fe3++3H2O,故答案为:Fe2O3+6H+=2 Fe3++3H2O;
(3)反应④的化学反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
点评 本题考查无机物推断,涉及铁及其化合物性质,难度不大,转化中反应现象为推断突破口,熟练掌握元素化合物性质即可解答.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

| 编号 | ① | ② | ③ | ④ |
| 稀硝酸的体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属的质量/g | 18.0 | 9.6 | 0 | 0 |
| NO 的体积/mL | 2240 | 4480 | 6720 | V |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 碳酸氢铵和足量的氢氧化钠溶液反应:NH4++OH-=NH3↑+H2O | |
| B. | 三氯化铁溶液中通入硫化氢气体:2Fe3++H2S=2Fe2++S↓+2H+ | |
| C. | 用稀硝酸浸泡做过银镜反应的试管:Ag+2H++NO3-=Ag++NO2↑+H2O | |
| D. | 偏铝酸钠溶液中通入过量的二氧化碳气体:2AlO2-+CO2+2H2O=2Al(OH)3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/mol•L-1 | 1 | 6 | 4 | x |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应②中的能量变化如图所示,则△H2=E1-E3 | |
| B. | N2的燃烧热为180 kJ•mol-1 | |
| C. | 由反应②知在温度一定的条件下,在一恒容密闭容器中通入1molN2和3molH2,反应后放出的热量为Q1kJ,则Q1=92.4 | |
| D. | 氨的催化氧化反应为4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=-906 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Mg(HCO3)2溶液中加入过量的 NaOH溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-↑+2H2O | |
| B. | FeBr2溶液中通入等物质的量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| C. | 苯酚与纯碱溶液反应:2C6H5OH+CO32-=CO2↑+H2O+2C6H5O- | |
| D. | 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该反应属于取代反应 | |
| B. | FeCl3溶液可用于区别香兰素与乙酸香兰酯 | |
| C. | 乙酸香兰酯的分子式为C10H12O4 | |
| D. | 乙酸香兰酯在足量NaOH溶液中水解得到乙酸钠和香兰素的钠盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com