
| A、N2 |
| B、NO |
| C、NO2 |
| D、HNO3 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 NaCl溶液 |
B、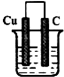 HCl溶液 |
C、 CuSO4溶液 |
D、 蔗糖溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子晶体中,共价键的键能越大,熔、沸点越高 |
| B、分子晶体中,共价键的键能越大,熔、沸点越高 |
| C、存在自由电子的晶体一定是金属晶体,存在阳离子的晶体一定是离子晶体 |
| D、离子晶体中可能存在共价键,分子晶体中可能存在离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、A原子最外层电子数比B原子的最外层电子数少 |
| B、A原子电子层数比B原子的电子层数多 |
| C、1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多 |
| D、常温时,A能从酸中置换出氢,而B不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,2.24L苯中含C-H数目为0.6 NA |
| B、常温下,9.2gNO2和N2O4的混合气体中含有的氮原子数目为0.2NA |
| C、常温下,1.0LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA |
| D、在反应KClO3+6HCl═KCl+3Cl2↑+3H2O中,每生成3molCl2转移的电子数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | Na+、Al 3+、Fe3+、Cu2+、Ba2+ |
| 阴离子 | OH-、Cl-、CO32-、NO3-、SO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 近年来,我国部分地区多次陷入严重雾霾之中,其中一个重要的原因是我国的能源消费结构以燃煤为主,改变煤的利用方式可减少环境污染.以下是对煤进行处理的方法:
近年来,我国部分地区多次陷入严重雾霾之中,其中一个重要的原因是我国的能源消费结构以燃煤为主,改变煤的利用方式可减少环境污染.以下是对煤进行处理的方法:| 反应过程 | 化学方程式 | △H(kJ?mol-1) |
| 甲醇合成反应 | 2H2(g)+CO(g)═CH3OH(g) | -90.8 |
| 水煤气变换反应 | CO(g)+H2O(g)═CO2(g)+H2(g) | -41.3 |
| 甲醇脱水反应 | 2CH3OH(g)═CH3OCH3(g)+H2O(g) | -23.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com