
| A、铁壳轮船在河水中航行比在海水中航行更易被腐蚀 |
| B、常温下,铁易被干燥的氯气腐蚀 |
| C、钢铁发生吸氧腐蚀时,发生的负极反应为02+4e-+2H20═40H- |
| D、为了防止枪炮表面的钢铁被腐蚀,可以在钢铁表面进行烤蓝处理 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
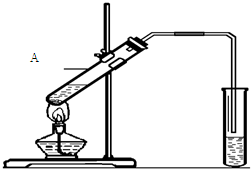 乙酸是食醋的主要成分,它具有以下化学性质:
乙酸是食醋的主要成分,它具有以下化学性质:查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y | Z | |
| ① | NaOH溶液 | KAlO2 | 稀硫酸 |
| ② | KOH溶液 | NaHCO3 | 浓盐酸 |
| ③ | O2 | N2 | H2 |
| ④ | FeCl3溶液 | Cu | 浓硝酸 |
| A、①③ | B、①④ | C、②④ | D、②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入少量的CH3COONa固体 |
| B、加入少量NaOH固体 |
| C、加入少量NaHCO3固体 |
| D、通入少量HCl气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升温增压 | B、降温增压 |
| C、升温减压 | D、降温减压 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、新制的氯水呈浅黄绿色,久置的氯水无色 |
| B、新制的氯水漂白作用强,久置的氯水漂白作用很弱或消失 |
| C、新制的氯水中没有氯离子,久置的氯水中才含有氯离子 |
| D、新制的氯水中含氯气多,久置的氯水中含有极少量的氯气或不含氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、测定同浓度的盐酸、硼酸溶液的导电能力 |
| B、常温下,用pH计测定硼酸钠溶液的pH |
| C、将碳酸钠溶液滴入硼酸溶液中,无明显现象 |
| D、将硼酸溶液稀释2倍后,用pH试纸测定其pH变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com