
| A、FeCl3溶液与Cu反应:Fe3++Cu═Fe2++Cu2+ |
| B、硫酸溶液与氢氧化钡溶液混合:SO42-+Ba2+═BaSO4↓ |
| C、用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-=Mn2++Cl2+2H2O |
| D、Cu溶于足量浓硝酸:Cu+2NO3-+4H+═Cu2++2NO2↑+2H2O |


科目:高中化学 来源: 题型:
| A、其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短,当其他条件不变时,升高反应温度,化学反应速率加快 |
| B、工业制硫酸中,在SO3的吸收阶段,吸收塔里要装填瓷环,增大气液接触面积,使SO3的吸收速率增大 |
| C、在容积可变的密闭容器中发生反应:2NH3(g)?N2H4(l)+H2(g),把容积的体积缩小一半,正反应速率加快,逆反应速率减慢 |
| D、A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2~3滴FeCl3溶液,B试管中产生气泡快,当其他条件不变时,催化剂可以改变化学反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| D |
| D |
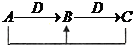
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=1的溶液中:Na+、Fe2+、NO3-、SO42- |
| B、c(OH-)=10-12的溶液中:NH4+、Al3+、NO3-、Cl- |
| C、由水电离的c(H+)=1×10-13mol?L-1的溶液中:Ba2+、K+、Cl-、[Al(OH)4]- |
| D、能使淀粉碘化钾试纸显蓝色的溶液:K+、SO42-、S2-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CuFeS2仅作还原剂,硫元素被氧化 |
| B、SO2是氧化产物,FeS是还原产物 |
| C、每生成1mol Cu2S,有4mol硫被氧化 |
| D、每转移1.2mol电子,有0.2mol硫被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2、SiO2、CO、P2O5均为酸性氧化物 |
| B、稀豆浆、硅酸、氯化铁溶液均为胶体 |
| C、空气、福尔马林、水玻璃、氨水均为混合物 |
| D、烧碱、冰醋酸、四氯化碳、石墨均为电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向Mg(OH)2悬浊液中加入FeCl3溶液:3OH-+Fe3+═Fe(OH)3↓ |
| B、淀粉碘化钾溶液在空气中变蓝:4I-+O2+2H2O=4OH-+2I2 |
| C、用酸性K2Cr2O7溶液检验酒精:3CH3CH2OH+2Cr2O72-+13H+=4Cr3++11H2O+3CH3COO- |
| D、次氯酸钠溶液中通入二氧化硫气体:2ClO-+SO2+H2O═2HClO+SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
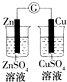
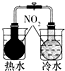
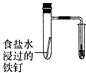
| A | B | C | D |
 |
 |
 |
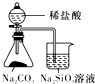 |
| 验证化学能转化为底电能 | 验证温度对平衡移动的影响 | 验证铁发生氢腐蚀 | 验证非金属Cl>C>Si |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com