
(1)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”(侯氏制碱法)两种工艺。
①“氨碱法”产生大量CaCl2废弃物,写出该工艺中产生CaCl2的化学方程式 ;
②写出“联合制碱法”有关反应的化学方程式________________。
③CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同______________________________________;
(2)钢铁工业对促进经济和社会发展起了重要作用。
① 炼钢时,加入硅、锰和铝的目的是_______________________。
② 不锈钢含有的Cr元素是在炼钢过程的氧吹____(填“前”或“后”)加入。
③ 炼铁和炼钢生产中,尾气均含有的主要污染物是________。从环保和经济角度考虑,上述尾气经处理可用作_________。
(1)①2NH4Cl+Ca(OH)2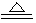 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
②NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl 2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
③氨碱法中的二氧化碳来源于石灰石的煅烧,联合制碱法中的二氧化碳来自于合成氨中工业中的废气。
(2)①脱氧调整钢的成分 ②后 ③ CO 燃料或还原剂
【解析】(1)①氨碱法中的回收氨而使石灰乳与副产物氯化铵反应,从而产生大量的废渣,2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
②联合制碱法的有关反应的化学方程式是:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl 2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
③氨碱法中的二氧化碳来源于石灰石的煅烧,联合制碱法中的二氧化碳来自于合成氨中工业中的废气。
(2)①炼钢时,加入硅、锰和铝的目的是脱氧调研钢的成分
②因为铬易被氧化,为了防止铬被氧化,不锈钢含的铬在炼钢的过程的吹氧后,如果在吹氧前加入铬,会形成炉渣而被除去。
③炼铁和炼钢的过程中,CO主要起的作用是还原剂,所以尾气中含有污染物CO,应对CO进行处理。


科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)1.1中和反应反应热的测定(解析版) 题型:选择题
下列说法正确的是( )
A.中和热一定是强酸跟强碱反应放出的热量
B.1 mol酸与1 mol 碱完全反应放出的热量是中和热
C.在稀溶液中,酸与碱发生中和反应生成1 mol H2O(l)时的反应热叫作中和热
D.测定中和热时可用稀硫酸和稀Ba(OH)2溶液
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学铁及其化合物主要性质(解析版) 题型:选择题
部分氧化的Fe?Cu合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理:
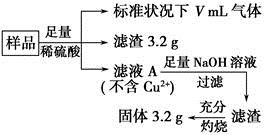
下列说法正确的是
A.滤液A中的阳离子为Fe2+、Fe3+、H+
B.样品中Fe元素的质量为2.24 g
C.样品中CuO的质量为4.0 g
D.V=896 mL
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学速率表示与平衡移动(解析版) 题型:选择题
已知反应4NH3+5O2 4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列正确的关系是
4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列正确的关系是
A.v(NH3)=v(O2) B.v(O2)=v(H2O)
C.v(NH3)=v(H2O) D.v(O2)=v(NO)
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学速率表示与平衡移动(解析版) 题型:选择题
T ℃时在2 L的密闭容器中X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,反应温度分别为T1和T2时,Y的体积分数与时间的关系如图2所示。则下列结论正确的是
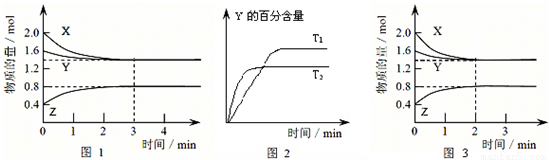 A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·(L·min)-1
A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·(L·min)-1
B.容器中发生的反应可表示为3X(g)+Y(g)  2Z(g)
2Z(g)
C.保持其他条件不变,升高温度,反应的化学平衡常数K减小
D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学选做题练习5(解析版) 题型:填空题
有机物A、B的分子式均为C10H10O5,均能发生如下变化。
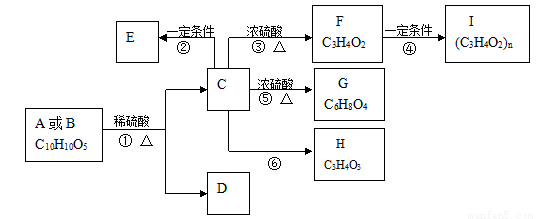
已知:
①A、B、C、D等均能与NaHCO3反应
②只有A、D能与FeCl3溶液发生显色反应,A苯环上的一溴代物只有两种
③F能使溴水褪色,
④H不能发生银镜反应
根据题意回答下列问题:
(1)反应③的反应类型是 ;有机物F含氧官能团的名称是 ;
(2)写出有机物的结构简式D 、H ;
(3)写出反应⑤的化学方程式 ;
(4)D的同分异构体有很多种,写出同时满足下列要求的所有同分异构体的结构简式 ;
①能与FeCl3溶液发生显色反应
②能发生银镜反应但不能水解
③苯环上的一卤代物只有2种
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学选做题练习4(解析版) 题型:填空题
水处理主要包括水的净化、污水处理、硬水软化和海水淡化等。
(1)水处理技术的核心是减少或除去水中的各种杂质离子。目前________和________是主要的去离子方法。
(2)ClO2是一种性能优良的消毒剂,可将废水中少量的S2-、NO2-和CN-等有毒有害的还原性离子氧化除去。请写出ClO2将废水中剧毒的CN-氧化成无毒气体的离子方程式________。
(3)地下水往往含有钙、镁的碳酸盐,自来水厂需要对地下水进行________处理。把进行过离子交換的CaR2(或MgR2)型树脂置于______中浸泡一段时间后便可再生。
(4)海水的淡化是除去海水中所含的盐分,右面是海水利用电渗析法获得淡水的原理图,已知海水中含有Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极。请回答:
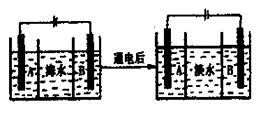
①阳离子交换膜是指________(填“A”或“B”)。
②写出通电后阳极区的电极反应式________________。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学选做题练习2(解析版) 题型:填空题
已知: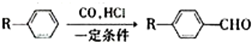
为合成某种液晶材料中间体M,有人提出如下不同的合成途径: 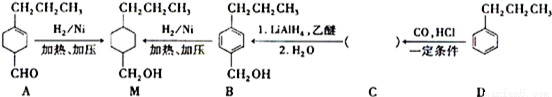
(1)常温下,下列物质能与A发生反应的有 (填序号)
a.苯 b.Br2/CCl4 c.乙酸乙酯 d.KMnO4/H+溶液
(2)M中官能团的名称是 ,由C→B反应类型 。
(3)由A催化加氢生成M的过程中,可能有中间生成物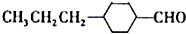 和 (写结构简式)生成。
和 (写结构简式)生成。
(4)检验B中是否含有C可选用试剂是 (任写一种名称)。
(5)物质B也可由C10H13Cl与NaOH水溶液共热生成,C10H13Cl的结构简式
(6)C的一种同分异构体E具有如下特点:
a.分子中含-OCH2CH3 b.苯环上只有两种化学环境不同的氢原子
写出E在一定条件下发生加聚反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学离子方程式的书写及正误判断(解析版) 题型:选择题
下列离子方程式书写正确的是
A.在100 mL浓度为1 mol·L-1的 Fe(NO3)3的溶液中通入足量SO2:2Fe3++SO2+2H2O=2Fe2++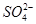 +4H+
+4H+
B.在100 mL浓度为2 mol·L-1的FeI2的溶液中通入标准状况下5.6 L的Cl2:4Fe2++6I-+5Cl2=4Fe3++3I2+10Cl-
C.向NaHCO3溶液中加入过量的澄清石灰水:2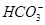 +Ca2++2OH-=CaCO3↓+2H2O+
+Ca2++2OH-=CaCO3↓+2H2O+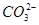
D.向明矾溶液中加入过量的氢氧化钡溶液:Al3++2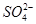 +2Ba2++4OH-=2BaSO4↓+
+2Ba2++4OH-=2BaSO4↓+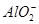 +2H2O
+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com