
| A.矿石在地下埋藏,铜矿最浅,容易开发,铝矿埋得深,难开发 |
| B.铜矿颜色较深,易发现,铝矿颜色较浅,不易发现 |
| C.铜矿较易还原,铝矿很难还原 |
| D.以上说法是错误的 |
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源:不详 题型:填空题
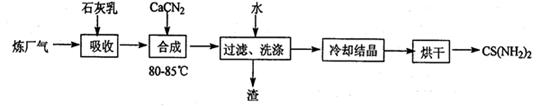
 2H2(g)+S2(g),其平衡常数表达式为K=。
2H2(g)+S2(g),其平衡常数表达式为K=。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.乙醇汽油是一种纯净物 |
| B.乙醇汽油作燃料不会产生碳氧化物等有害气体,其优点是可以减少对环境的污染 |
| C.乙醇和汽油都可作溶剂,也可相互溶解 |
| D.乙醇和乙二醇互为同系物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③④ | B.⑤⑥⑦⑧ | C.③④⑤⑥ | D.除①②外 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
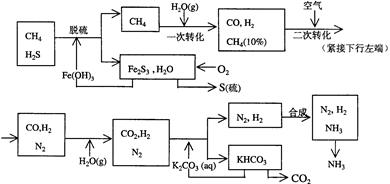
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
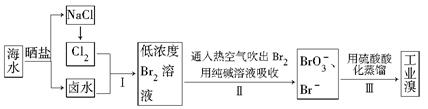

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
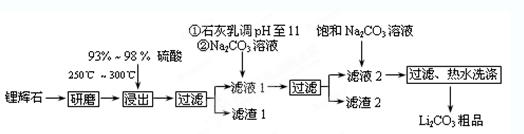
 Li2SO4+Al2O3·4SiO2·H2O↓
Li2SO4+Al2O3·4SiO2·H2O↓| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
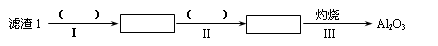
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
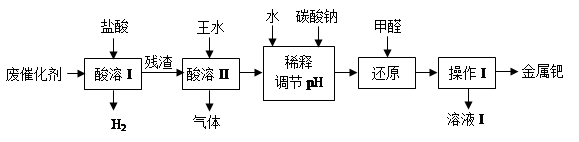
 3H2PdCl4 + 2NO↑+ 4H2O
3H2PdCl4 + 2NO↑+ 4H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com