
研究CO、SO2、NO等大气污染气体的综合处理与利用具有重要意义。
(1)以CO或CO2与H2为原料,在一定条件下均可合成甲醇,你认为用哪种合成设计线路更符合“绿色化学”理念:(用化学反应方程式表示) 。
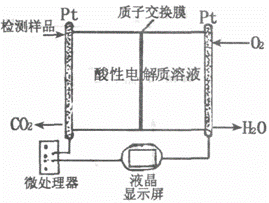
(2)右图所示是用于合成甲醇产品中甲醇含量的检测仪。写出该仪器工作时的电极反应式:
负极 ,正极 。
(3)一定条件下,NO2和SO2反应生成SO3(g)和NO两种气体,现将体积比为1:2的NO2和SO2的混合气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。(填序号)
A.体系压强保持不变 B.混合气体颜色保持不变
C.SO3、NO的体积比保持不变 D.每消耗 1 mol SO2,同时生成1 mol NO
当测得上述平衡体系中NO2与SO2体积比为1:6时,则该反应平衡常数K值为 ;
(4)工业常用Na2CO3饱和溶液回收NO、NO2气体:
NO+NO2+Na2CO3===2NaNO2+CO2 2NO2+Na2CO3===NaNO3+NaNO2+CO2
若用足量的Na2CO3溶液完全吸收NO、NO2混合气体,每产生标准状况下CO2 2.24L(CO2气体全部逸出)时,吸收液质量就增加4.4g,则混合气体中NO和NO2体积比为 。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
Ⅰ:某课外活动小组用如图装置进行实验,试回答下列问题。(1)若开始时开关K与a连接,则B极的电极反应式为 。
(2)若开始时开关K与b连接,则B极的电极反应式为
Ⅱ:下图A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
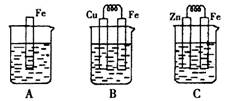
(3)B中若收集到224ml气体(标准状况),则溶解的金属质量为
(4)C中被腐蚀的金属是__________(填化学式),A、B、C中铁被腐蚀的速率,
 由快到慢的是顺序是_____________(用“>”表示)。
由快到慢的是顺序是_____________(用“>”表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
1,2-二溴乙烷可做汽油抗爆剂的添加剂,常温下它是无色液体,密度是2.18g/cm3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用下图所示装置制备1,2-二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。
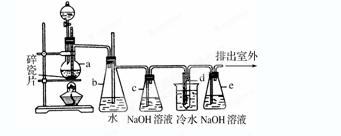
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式_____________________________。
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象________________________________________。
(3)容器c中NaOH溶液的作用是: 。
(4)某学生做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量比正常情况下超出许多,如果装置的气密性没有问题,试分析其可能的原因: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验的操作、现象和解释或结论都正确的是
| 操作 | 现象 | 解释或结论 | |
| A | 向装有Fe(NO3)2溶液的试管中加入几滴稀H2SO4 | 溶液颜色基本不变 | Fe(NO3)2与H2SO4不反应 |
| B | 向饱和Na2CO3溶液中通入足量CO2 | 溶液变浑浊 | 析出了NaHCO3晶体 |
| C | 将Al2(SO4)3溶液蒸干 | 有白色固体生成 | Al3++3H2O |
| D | 将Na放入CuSO4溶液中 | 有红色固体析出 | 2Na+Cu2+===Cu+2Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
CH3CH(C2H5)CH(CH3)2的名称是
A. 1,3-二甲基戊烷 B.2-甲基-3-乙基丁烷
C.3,4-二甲基戊烷 D.2,3-二甲基戊烷
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列事实不能说明上述观点的是
A.苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应
B.甲苯能使酸性高锰酸钾溶液褪色,乙烷、苯不能使酸性高锰酸钾溶液褪色
C.乙烯能发生加成反应,乙烷不能发生加成反应
D.苯与硝酸在加热时发生取代反应,甲苯与硝酸在常温下就能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
为纪念编制了第一个元素周期表的俄国化学家门捷列夫,人们把第101号元素(人工合成元素)命名为钔。下列关于了258Md和260Md的叙述正确的是
A.258Md原子所含中子数与质子数之差为56
B.258Md和260Md互称为同素异形体
C.258Md和260Md为同一种核素
D.有一种Md元素的相对原子质量为258
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:H+(aq) + OH-(aq) == H2O(l) ;ΔH = -57.3 kJ/mol。
(1)0.1 mol Ba(OH)2配成稀溶液,跟足量的稀硝酸反应,能放出 kJ热量;
(2)用10.0 L 0.10 mol/LCH3COOH溶液与20.0 L 0.10 mol/L NaOH溶液反应,放出的热量
(选填“大于”、“小于”或“等于”)57.3 kJ,理由是 ;
(3)用2 L 0.5 moL/L的H2SO4与1 L 1 mol/L的NaOH溶液反应,放出的热量
(选填“大于”、“小于”或“等于”)57.3 kJ,理由是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com