
【题目】2mol金属钠和1mol氯气反应的能量关系如图所示,下列说法不正确的( )

A.△H2+△H3+△H4+△H5+△H6+△H7=△H1
B.△H4的值数值上和Cl-Cl共价键的键能相等
C.△H5<0,在相同条件下,2Br(g)的△H5′<△H5
D.△H7<0,且该过程形成离子键
 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】已知:反应CO(g)+H2O(g)![]() CO2(g)+H2(g)在不同的温度下的平衡常数分别为:
CO2(g)+H2(g)在不同的温度下的平衡常数分别为:
t/℃ | 700 | 800 | 830 | 1000 | 1200 |
k | 1.67 | 1.11 | 1.00 | 0.60 |
下列有关叙述不正确的是
A. 该反应平衡常数表达式为K=[c(CO2)·c(H2)]/[c(CO)·c(H2O)]
B. 该反应的逆反应是吸热反应
C. 830℃时,向恒容密闭容器中加入CO2 和H2各1mol,当测得CO2 的物质的量为0.4mol时,反应处于平衡状态
D. 若某温度下该反应中各物质的平衡浓度符合关系式:[c(CO2)/3c(CO)]=[c(H2O)/5c(H2)],则该温度是1000 C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.1000 mol/L NaOH溶液滴定未知浓度的盐酸溶液,操作可分解为如下几步:
A.用蒸馏水洗干净滴定管;B. 用待测定的溶液润洗酸式滴定管;C.用酸式滴定管取稀盐酸20.00 mL,注入锥形瓶中,加入酚酞;D.另取锥形瓶,再重复操作一次;E.检查滴定管是否漏水;F.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管“0”刻度以上2~3 cm处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下;
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。完成以下填空:
(1)正确操作的顺序是(用序号字母填写)_____________。
(2)操作F中应该选择图中________滴定管(填标号)。
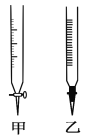
(3)滴定时边滴边摇动锥形瓶,眼睛应观察________。
A. 滴定管内液面的变化 B. 锥形瓶内溶液颜色的变化
滴定终点溶液颜色的变化是____________________________。
(4)滴定结果如表所示:
滴定次数 | 待测溶液体积/mL | 标准溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 20 | 1.02 | 21.03 |
2 | 20 | 2.00 | 25.00 |
3 | 20 | 0.60 | 20.60 |
滴定中误差较大的是第________次实验,造成这种误差的可能原因是________。
A. 碱式滴定管在装液前未用标准NaOH溶液润洗2~3次
B. 滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C. 滴定开始前碱式滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
D. 达到滴定终点时,仰视溶液凹液面最低点读数
E. 滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
(5)该盐酸的浓度为________mol/L。
(6)如果准确移取20.00 mL 0.1000 mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,是否也可测定出盐酸的物质的量浓度?________(填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:aHClO3═bO2↑+cCl2↑+dHClO4+eH2O,用湿润的淀粉碘化钾试纸检验气体产物时,试纸先变蓝后褪色。下列说法正确的是( )
A.由反应可确定:氧化性:HClO4>HClO3
B.变蓝的淀粉碘化钾试纸褪色是因为可能发生了:4Cl2+I2+6H2O═12H++8Cl-+2IO3-
C.若氯酸分解所得混合气体,1 mol混合气体质量为47.6 g,则反应方程式可表示为26HClO3 ═15O2↑+8Cl2↑+10HClO4+8H2O
D.若化学计量数a=8,b=3,则该反应转移电子数为20e-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,常温时将一滴管液体Y一次性全部挤到充满O2的锥形瓶内(装置气密性良好),若锥形瓶内气体的最大物质的量是a mol,久置后其气体的物质的量是b mol,不存在a>b关系的是( )
X | Y |
| |
A | 过量C、Fe碎屑 | 稀HCl | |
B | 过量Na2CO3粉末 | 稀H2SO4 | |
C | 过量Fe、Al碎屑 | 浓H2SO4 | |
D | 过量Cu、CuO粉末 | 浓HNO3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中是在实验室进行氨气快速制备与性质探究实验的组合装置,部分固定装置未画出。

(1)在组装好装置后,若要检验A~E装置的气密性,其操作是:首先______________,打开弹簧夹1,在E中装入水,然后微热A,观察到E中有气泡冒出,移开酒精灯,E中导管有水柱形成,说明装置气密性良好。
(2)装置B中盛放的试剂是______________________。
(3)点燃C处酒精灯,关闭弹簧夹2,打开弹簧夹1,从分液漏斗放出浓氨水至浸没烧瓶中固体后,关闭分液漏斗活塞,稍等片刻,装置C中黑色固体逐渐变红,装置E中溶液里出现大量气泡,同时产生_____________(填现象)。从E中逸出液面的气体可以直接排入空气,写出C中反应的化学方程式:_______。
(4)当C中固体全部变红色后,关闭弹簧夹1,慢慢移开酒精灯,待冷却后,称量C中固体质量,若反应前固体质量为16 g,反应后固体质量减少2.4 g,通过计算确定该固体产物的化学式:______。
(5)在关闭弹簧夹1后,打开弹簧夹2,残余气体进入F中,很快发现装置F中产生白烟,同时发现G中溶液迅速倒吸流入F中。写出产生白烟的化学方程式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铁矿(主要成分FeS2)是工业制硫酸的主要原料,暴露在空气中会被缓慢氧化,其氧化过程如图所示。

(1)写出a步骤离子方程式________
(2)如何检验b步骤反应后的溶液中含Fe2+________
(3)取10mLb步骤反应后的溶液测定其成分,通入标准状况下Cl222.4mL恰好完全反应。然后调节pH,使溶液中的铁元素全部转化为沉淀,经过滤、洗涤、灼烧,冷却后称重,得固体质量为0.32g,则该溶液中c(Fe3+)=________(写出计算推理过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 时,向
时,向![]() 中不断滴入
中不断滴入![]() ,混合溶液pH变化如图所示。此过程溶液下列说法不正确的是
,混合溶液pH变化如图所示。此过程溶液下列说法不正确的是![]() 已知:
已知:![]() 时一元酸
时一元酸![]() 电离平衡常数
电离平衡常数![]()

A.a点溶液的pH大于3
B.b点溶液中离子:![]()
C.c点表示酸![]() 和
和![]() 溶液恰好完全反应
溶液恰好完全反应
D.d点溶液加水稀释后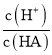 的值会增大
的值会增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积一定的密闭容器中![]() 和3mol
和3mol![]() 发生反应:
发生反应:![]()
![]()
![]() 。下列有关说法正确的是
。下列有关说法正确的是
A.降低温度可以加快反应速率
B.向容器中再加入![]() 可以加快反应速率
可以加快反应速率
C.达到化学反应限度时,生成2mol![]()
D.达到化学平衡时![]() 、
、![]() 、
、![]() 的物质的量之比为1:3:2
的物质的量之比为1:3:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com