
氮化钠(Na3N)是一种实施管制的化学品,它是科学家制备的一种重要的化合物,与水作用可产生NH3。
请回答下列问题:
(1)Na3N的电子式是____________,该化合物是由________键形成的。
(2)Na3N与盐酸反应生成________种盐,其电子式分别是________。
(3)Na3N与水的反应属于________(填基本反应类型)反应。
(4)比较Na3N中两种微粒的半径:
r(Na+)________r(N3-)(填“>”“=”或“<”)。
 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源:2014学年高一化学人教版必修2 2.3.1化学反应的速率练习卷(解析版) 题型:选择题
硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,下列各组实验中最先出现浑浊的是( )。
实验反应温度/℃Na2S2O3溶液稀H2SO4H2O
V/mLc/(mol·L-1)V/mLc/(mol·L-1)V/mL
A2550.1100.15
B2550.250.210
C3550.1100.15
D3550.250.210
查看答案和解析>>
科目:高中化学 来源:2014学年高一化学人教版必修2 2.1化学能与热能练习卷(解析版) 题型:选择题
如图所示,把下列物质分别加入装有水的锥形瓶里,立即塞紧带有U形管的塞子,已知U形管内预先装有少量水(为方便观察,预先将水染成红色),结果U形管左边液面升高,则加入的物质可能是 ( )。

A.NaOH固体 B.浓硫酸 C.NH4NO3晶体 D.Na2O2固体
查看答案和解析>>
科目:高中化学 来源:2014学年高一化学人教版必修2 1章物质结构 元素周期律练习卷(解析版) 题型:选择题
已知铍的原子序数为4,下列对铍及其化合物的叙述中,正确的是( )。
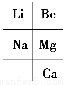
A.铍的金属性比钠强
B.氯化铍的氧化性比氯化锂弱
C.氢氧化铍的碱性比氢氧化钙弱
D.单质铍易跟冷水反应生成H2
查看答案和解析>>
科目:高中化学 来源:2014学年高一化学人教版必修2 1章物质结构 元素周期律练习卷(解析版) 题型:选择题
下列说法中不正确的是( )。
A.离子化合物中不一定含有金属元素
B.由不同原子所形成的纯净物一定是化合物
C.在含有阳离子的化合物中,一定含有阴离子
D.含有金属元素的离子不一定是阳离子
查看答案和解析>>
科目:高中化学 来源:2014学年高一化学人教版必修2 1.3化学键练习卷(解析版) 题型:选择题
下列物质中,既含离子键、又含共价键的是( )。
A.NaOH B.Na2O C.H2O D.CaCl2
查看答案和解析>>
科目:高中化学 来源:2014学年高一化学人教版必修2 1.3化学键练习卷(解析版) 题型:选择题
下列哪一组元素的原子间反应容易形成离子键( )。
原子 | a | b | c | d | e | f | g |
M层电子数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
①a和c ②a和f ③d和g ④b和g
A.①② B.②④ C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源:2014学年高一化学人教版必修2 1.2.1电子的排布元素周期律练习卷(解析版) 题型:选择题
根据下表信息,判断以下叙述正确的是 ( )。
部分短周期元素的原子半径及主要化合价
元素代号 | L | M | Q | R | T |
原子半径/nm | 0.166 | 0.143 | 0.112 | 0.104 | 0.066 |
主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.氢化物的沸点为H2T<H2R B.单质与稀盐酸反应的速率为L<Q
C.M与T形成的化合物具有两性 D.L2+与R2-的核外电子数相等
查看答案和解析>>
科目:高中化学 来源:2014学年高一化学人教版必修2 1.1.1元素周期表练习卷(解析版) 题型:选择题
在现行元素周期表中,所含元素种数最多的族和周期分别是( )。
A.第ⅠA族 第六周期 B.第Ⅷ族 第六周期
C.第ⅢB族 第六周期 D.第ⅢA族 第六周期
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com