


分析 制备聚铁和绿矾(FeSO4•7H2O)流程为:硫酸厂烧渣与硫酸、氧气反应,得到滤液X和不溶物(S、二氧化硅等)W;滤液X中进入铁粉生成硫酸亚铁溶液,硫酸亚铁溶液通过浓缩蒸发、冷却结晶得到绿矾;将滤液X通过调节pH获得溶液Z,在70~80℃条件下得到聚铁聚铁,最后得到聚铁,
(1)利用实验仪器的连接,安全瓶的使用以及尾气吸收来分析;
(2)此题为二氧化硫的验证,利用其特殊性质漂白性来分析;
(3)利用二价铁与三价铁之间的相互转化来分析;
(4)利用pH试纸测定溶液酸碱性的方法来分析.
解答 解:制备聚铁和绿矾(FeSO4•7H2O)流程为:硫酸厂烧渣与硫酸、氧气反应,得到滤液X和不溶物(S、二氧化硅等)W;滤液X中进入铁粉生成硫酸亚铁溶液,硫酸亚铁溶液通过浓缩蒸发、冷却结晶得到绿矾;将滤液X通过调节pH获得溶液Z,在70~80℃条件下得到聚铁聚铁,最后得到聚铁,
(1)收集二氧化硫应先干燥再收集.二氧化硫的密度比空气大,要从c口进气,最后进行尾气处理.因为二氧化硫易于氢氧化钠反应,故D的作用是安全瓶,防止倒吸;E的作用为尾气处理,
故答案为:d;e;c;b;安全瓶,防止倒吸;尾气处理,防止污染;
(2)检验二氧化硫的一般方法是:将气体通入品红溶液中,如果品红褪色,加热后又恢复红色,证明有二氧化硫.
故答案为:将气体通入品红溶液中,如果品红褪色,加热后又恢复红色,证明有二氧化硫;
(3)因为在烧渣中加入了硫酸和足量氧气,故溶液Y中含有Fe3+,故应先加入过量的铁粉,然后过滤,
故答案为:铁粉;
(4)用pH试纸测定方法为:将试纸放在表面皿上,用洁净的玻璃棒蘸取待测液,点在试纸的中央,然后与标准比色卡对比.氢氧化铁的含量比硫酸亚铁高,若溶液Z的PH偏小,则聚铁中生成的氢氧根的含量减少,使铁的含量减少,
故答案为:将试纸放到表面皿上,用洁净的玻璃棒蘸取少许待测液,滴在试纸的中央.然后与标准比色卡对比;偏低.
点评 本题借助于实验考查基础知识达到了很好的效果.对学生来说聚铁不是很熟悉,但是铁与亚铁之间的转化还是很容易实现的,起点高,落点低,是一好题,题目难度中等.


科目:高中化学 来源: 题型:填空题
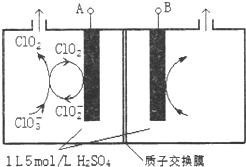 二氧化氯(ClO2)是国内外公认的高效、广谱、快速、安全无毒的杀菌消毒剂,被称为“第4代消毒剂”.工业上可采用氯酸钠(NaClO3)或亚氯酸钠(NaClO2)为原料制备ClO2.
二氧化氯(ClO2)是国内外公认的高效、广谱、快速、安全无毒的杀菌消毒剂,被称为“第4代消毒剂”.工业上可采用氯酸钠(NaClO3)或亚氯酸钠(NaClO2)为原料制备ClO2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 序号 | 操作 | 可能出现的现象 | 结论 |
| ① | 向a试管中滴加几滴0.01mol/L的KMnO4(或溴水)溶液 | 若溶液褪色 | 则假设1成立 |
| 若溶液不褪色 | 则假设2或3成立 | ||
| ② | 向b试管中滴加几滴品红溶液 | 若溶液褪色 | 则假设1或3成立 |
| 若溶液不褪色 | 假设2成立 | ||
| ③ | 向C试管中滴加几滴淀粉-KI溶液 | 若溶液变为蓝色 | 假设3成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH固体 | B. | NaCl固体 | C. | MgSO4固体 | D. | NaHSO4固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知某可逆反应:mA(气)+nB(气)?xC(气)△H=QkJ•mol-1,在密闭容器中进行,如图表示反应在不同时间t,温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则( )
已知某可逆反应:mA(气)+nB(气)?xC(气)△H=QkJ•mol-1,在密闭容器中进行,如图表示反应在不同时间t,温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则( )| A. | T1>T2,P1>P2,m+n>x,Q>0 | B. | T1>T2,P1<P2,m+n<x,Q<0 | ||
| C. | T1>T2,P1<P2,m+n<x,Q>0 | D. | T1<T2,P1>P2,m+n>x,Q<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com