
【题目】下列物质中,既能跟盐酸反应,又能跟NaOH溶液反应的是( )
A.NaHCO3
B.Fe2O3
C.Al2O3
D.SiO2
 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t℃时AgCl的Ksp=4×10-10,下列说法不正确的是

A. 在t℃时,AgBr的Ksp为4.9×10-13
B. 在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点
C. 图中a点对应的是AgBr的不饱和溶液
D. 在t℃时,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)平衡常数K≈816
AgBr(s)+Cl-(aq)平衡常数K≈816
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用提取粗盐后的盐卤(主要成分为MgCl2)制备金属镁,其工艺流程如下,下列说法中,错误的是( )
![]()
A. 操作①发生的反应为非氧化还原反应
B. 若在实验室进行操作①只需要漏斗和烧杯两种玻璃仪器
C. 操作②是蒸发浓缩结晶
D. 在整个制备过程中,未发生置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】aLCO2气体通过足量Na2O2后,所得气体再与bLNO混合时,可得到cL气体(气体体积均在相同状况下测定),下列表达式中,错误的是( )
A. 若a则c<![]() (a+b) B. 若a则c>
(a+b) B. 若a则c>![]() (a+b)
(a+b)
C. 若a>b则c=![]() (a+b) D. 若a=b则c=
(a+b) D. 若a=b则c=![]() (a+b)
(a+b)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子或离子中中心原子价层电子对几何构型为四面体且分子或离子空间构型为V形的是( )
A. NH B. PH3 C. OF2 D. H3O+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、有一瓶澄清的溶液,其中可能含有H+、NH4+、Mg2+、Ba2+、Al3+、I﹣、NO3﹣、CO32﹣、SO42﹣、AlO2﹣,取该溶液进行以下实验:
(1)取pH试纸检验,溶液呈酸性,可以排除______________的存在.
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4呈紫红色,可以排除_______存在.
(3)另取出部分溶液逐渐加入NaOH溶液,使溶液从酸性逐渐变为碱性,反应过程中均无沉淀产生,则又可排除____________的存在.
(4)取出部分上述碱性溶液加Na2CO3溶液后,有白色沉淀生成,证明有_______的存在,又可以排除__________的存在.
(5)根据上述实验事实可以确定,该溶液中肯定存在的离子是____________,还不能确定是否存在的离子是_______________.
Ⅱ、某混合物 A,含有 KAl(SO4)2、Al2O3 和 Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
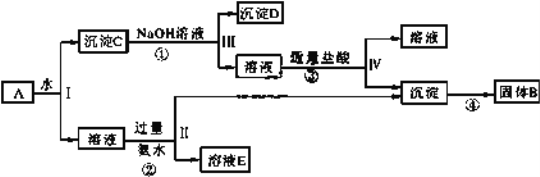
据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是__________。
(2)根据上述框图反应关系,写出下列B、C、D 所含物质的化学式(提示:可为混合物)。
固体 B_________;沉淀 C__________;沉淀 D _________;
(3)写出①、②反应离子方程式。
①___________________________________________;
②___________________________________________;
(4)步骤③较难操作,如何将实验方案进行改进?________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以反应 5H2C2O4+2MnO4 -+6H+ = 10CO2↑+ 2Mn2+ + 8H2O 为例探究“外界条件对化学反应速率的影响”。实验时,分别量取 H2C2O4 溶液和酸性 KMnO4溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。
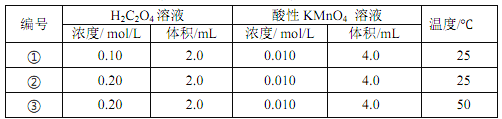
下列说法不正确的是
A. 实验①、 ②、 ③所加的H2C2O4 溶液均要过量
B. 若实验①测得 KMnO4溶液的褪色时间为 40 s, 则这段时间内平均反应速率 v(KMnO4)= 2. 5×10-4 mol/L/s
C. 实验①和实验②是探究浓度对化学反应速率的影响, 实验②和③是探究温度对化学反应速率的影响
D. 实验①和②起初反应均很慢,过了一会儿速率突然增大,可能是生成的 Mn2+对反应起催化作用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com