
【题目】A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是________(填元素符号),其中C原子的核外电子排布式为__________________。
(2)单质A有两种同素异形体,其中沸点高的是______(填分子式),原因是__________________________________________;A和B的氢化物所属的晶体类型分别为________和________。
(3)C和D反应可生成组成比为1∶3的化合物E,E的立体构型为______________,中心原子的杂化轨道类型为________。
(4)化合物D2A的立体构型为________,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为_______________________________________________。
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566 nm,F的化学式为________;晶体F的密度(g·cm-3 )________________________________。(列出表达式)
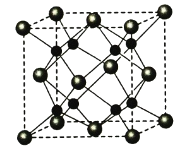
【答案】O1s22s22p63s23p3O3相对分子质量越大,熔沸点越高分子晶体离子晶体三角锥形sp3V形2Cl2+Na2CO3=Cl2O↑+2NaCl+CO2↑Na2O![]()
【解析】
C核外电子总数是最外层电子数的3倍,应为P元素,C、D为同周期元素,则应为第三周期元素,D元素最外层有一个未成对电子,应为Cl元素,A2﹣和B+具有相同的电子构型,结合原子序数关系可知A为O元素,B为Na元素。
(1)同周期自左而右电负性增大,Cl元素氧化物中氧元素表现负价,四种元素电负性最大的为O元素;C为P元素,原子核外电子数为15,根据能量最低原理原理书写核外电子排布式;(2)A为O元素,有O2、O3两种同素异形体,均属于分子晶体,相对原子质量越大,沸点越高;A、B的氢化物分别为H2O、NaH,前者为分子晶体、后者为离子晶体;(3)C和D生成组成比为1:3的化合物E为PCl3,计算P原子价层电子对数、孤电子对数,确定杂化方式与空间构型;(4)A和B能够形成化合物F为离子化合物,阴离子位于晶胞的定点和面心,阳离子位于晶胞的体心,则Na的个数为8,O的个数为8×![]() +6×
+6×![]() =4,N(Na):N(O)=2:1,则形成的化合物为Na2O,由晶胞结构可知B原子配位数为4,计算晶胞质量和体积,可计算密度。
=4,N(Na):N(O)=2:1,则形成的化合物为Na2O,由晶胞结构可知B原子配位数为4,计算晶胞质量和体积,可计算密度。
(1)四种元素分别为O、Na、P、Cl,电负性最大的为O元素,C为P元素,核外电子排布为1s22s22p63s23p3。(2)A为O元素,有O2、O3两种同素异形体,二者对应的晶体都为分子晶体,因O3相对分子质量较大,则范德华力较大,沸点较高,A的氢化物为水,为分子晶体,B的氢化物为NaH,为离子晶体。(3)C和D反应可生成组成比为1:3的化合物为PCl3,P形成3个δ键,孤电子对数为![]() ,则P原子为sp3杂化,立体构型为为三角锥形;(4)化合物D2A为Cl2O,O为中心原子,形成2个δ键,孤电子对数为
,则P原子为sp3杂化,立体构型为为三角锥形;(4)化合物D2A为Cl2O,O为中心原子,形成2个δ键,孤电子对数为![]() ,则中心原子的价层电子对数为4,立体构型为V形;氯气与湿润的Na2CO3反应可制备Cl2O,反应的方程式为2Cl2+Na2CO3+H2O=Cl2O↑+2NaCl+CO2↑。(5)A和B能够形成化合物F为离子化合物,阴离子位于晶胞的定点和面心,阳离子位于晶胞的体心,则Na的个数为8,O的个数为8×
,则中心原子的价层电子对数为4,立体构型为V形;氯气与湿润的Na2CO3反应可制备Cl2O,反应的方程式为2Cl2+Na2CO3+H2O=Cl2O↑+2NaCl+CO2↑。(5)A和B能够形成化合物F为离子化合物,阴离子位于晶胞的定点和面心,阳离子位于晶胞的体心,则Na的个数为8,O的个数为8×![]() +6×
+6×![]() =4,N(Na):N(O)=2:1,则形成的化合物为Na2O;晶胞的质量为
=4,N(Na):N(O)=2:1,则形成的化合物为Na2O;晶胞的质量为![]() ,晶胞的体积为(0.566×10-7)3cm3,则晶体F的密度的计算式为
,晶胞的体积为(0.566×10-7)3cm3,则晶体F的密度的计算式为
![]() 。
。


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】常温下,现向50 mL 0.1 mol·L-1 NH4HSO4溶液中滴加0.05 mol·L-1 NaOH溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生)。下列说法正确的是

A.b点溶液中离子浓度由大到小的顺序为:c(Na+)>c(SO![]() )>c(NH
)>c(NH![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
B.图中b、c、d三点溶液中水的电离程度最大的是c点
C.b点后滴加NaOH溶液过程中,NH3·H2O的电离程度逐渐减小
D.pH=7时,溶液中c(H+)+c(Na+)+c(NH![]() )=c(SO
)=c(SO![]() )+c(OH-)
)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
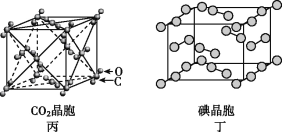
【题目】有关晶体的结构如图所示,下列说法中不正确的是
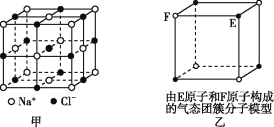
A. 在NaCl晶体(图甲)中,距Na+最近的Cl-形成正八面体
B. 该气态团簇分子(图乙)的分子式为EF或FE
C. 在CO2晶体(图丙)中,一个CO2分子周围有12个CO2分子紧邻
D. 在碘晶体(图丁)中,存在非极性共价键和范德华力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符合的是

A.图甲表示燃料燃烧反应的能量变化
B.图乙表示酶催化反应的反应速率随反应温度的变化
C.图丙表示弱电解质在水中建立电离平衡的过程
D.图丁表示强碱滴定强酸的滴定曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子是( )
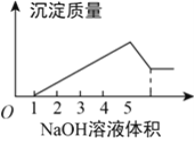
A. Mg2+、Al3+、Ba2+ B. H+、Mg2+、Al3+
C. H+、Cu2+、Al3+ D. 只有Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列三组液体:①75%的乙醇溶液;②氯化钠溶液和四氯化碳组成的混合液;③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
A.分液、萃取、蒸馏B.蒸馏、分液、结晶
C.分液、结晶、萃取D.蒸馏、分液、萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中对应关系正确的是
A | CH3CH3+Cl2 | 均为取代反应 |
B | 由油脂得到甘油 | 均发生了水解反应 |
C | Cl2+2Br=2Cl+Br2 | 均为单质被还原的置换反应 |
D | 2Na2O2+2H2O+4NaOH+O2↑ | 均为水作还原剂的氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 摩尔是国际科学界建议采用的一种物理量
B. 0.012 kg 12C中所含的碳原子数为NA
C. 物质的摩尔质量等于其相对分子(原子)质量
D. 1 mol任何物质都含有约6.02×1023个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在日常生产生活中应用广泛,研究铁及其化合物的应用意义重大。
(1)所含铁元素只有还原性的物质是_________。
A.Fe B.FeCl2 C.FeCl3 D.Fe2O3
(2)当人体缺铁时,往往需要吃补铁保健品。人体能够吸收的是+2价的铁,但是+2价的铁很容易被氧化。
①如何检验某固体补铁剂中铁元素已被氧化?写出操作过程、现象及结论。
答:____________________________________________________________________。
②服用维生素C,可使食物中的三价铁离子转化为二价铁离子。由此可推知,维生素C具有________________(填化学性质)。
(3) 高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、C1O-、OH-、FeO42-、Cl-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:_____Fe(OH)3+_____ClO-+_________=_____FeO42-+_____Cl-+_________
(4)工业上用氯化铁腐蚀铜箔、制造电路板。某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:
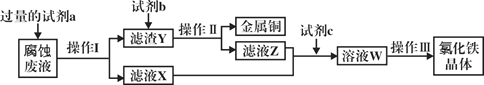
回答下列问题:
①试剂a是___________,操作I用到的玻璃仪器有烧杯、玻璃棒和___________。
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为___________。
③上述流程中操作III包括________________、________________、过滤、洗涤。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com