
| A. | 在稀氨水中通入过量CO2:NH3•H2O+CO2═NH4++HCO3- | |
| B. | 向(NH4)2SO4溶液中加入适量Ba(OH)2:Ba2++SO42-=BaSO4↓ | |
| C. | 用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ | |
| D. | 氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-═CaSO4↓+H2O |
分析 A.反应生成碳酸氢铵;
B.漏写生成一水合氨的离子反应;
C.发生氧化还原反应生成硝酸铁、NO、S和水;
D.不符合离子的配比.
解答 解:A.在稀氨水中通入过量CO2的离子反应为NH3•H2O+CO2═NH4++HCO3-,故A正确;
B.向(NH4)2SO4溶液中加入适量Ba(OH)2的离子反应为2NH4++2OH-+Ba2++SO42-=BaSO4↓+2NH3•H2O,故B错误;
C.用稀HNO3溶解FeS固体的离子反应为NO3-+FeS+4H+═Fe3++S↓+NO↑+2H2O,故C错误;
D.氢氧化钙溶液与等物质的量的稀硫酸混合的离子反应为Ca2++2OH-+2H++SO42-═CaSO4↓+2H2O,故D错误;
故选A.
点评 本题考查离子反应方程式书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.


科目:高中化学 来源: 题型:解答题
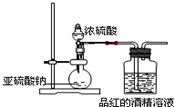 为探究SO2的漂白是SO2直接作用于有色物质,还是SO2与水反应的产物的作用,设计如图装置进行实验:(图中所用硫酸的质量分数为70%)
为探究SO2的漂白是SO2直接作用于有色物质,还是SO2与水反应的产物的作用,设计如图装置进行实验:(图中所用硫酸的质量分数为70%)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
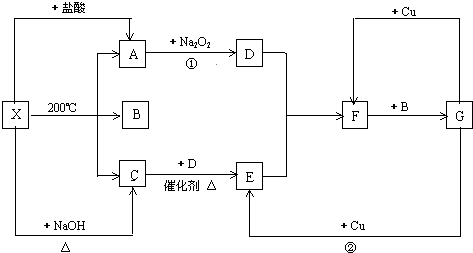
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
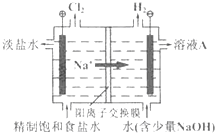 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.完成下列填空:
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.完成下列填空:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大O2的浓度可以提高反应速率和SO2的转化率 | |
| B. | 使用催化剂可以提高SO2的转化率 | |
| C. | 反应在450℃时的平衡常数小于500℃时的平衡常数 | |
| D. | 2moLSO2(g)和1moLO2(g)所含的总能量小于2moLSO3(g)所含的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
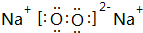 ,其中含有的化学键为离子键和共价键.
,其中含有的化学键为离子键和共价键.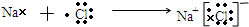 .
. 查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn是正极,Ag2O是负极 | B. | 负极反应为Zn+2OH--2e-=Zn(OH)2 | ||
| C. | 工作时负极区溶液的pH增大 | D. | 工作时溶液中K+移向负极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com