
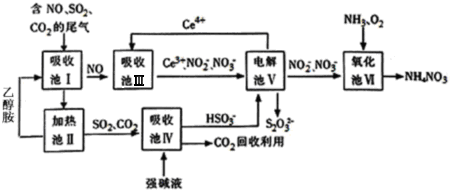
分析 由流程可知,吸收池I中发生SO2+OH-=HSO3-、CO2+OH-=HCO3-,NO不反应,吸收池Ⅲ中,酸性条件下NO转化为NO2-,发生NO+H2O+Ce4+=Ce3++NO2-+2H+,吸收池Ⅳ中NaHSO3溶液中HSO3-的电离大于水解,HSO3-?SO32-+H+,溶液显示酸性,加入CaCl2溶液后,Ca2++SO32-=CaSO3↓使电离平衡右移,电解池Ⅴ可使Ce4+再生,Ce失去电子在阳极得到,阴极上发生2HSO3-+4H++4e-=S2O32-+3H2O,氧化池Ⅵ中得到粗产品NH4NO3,NO2-完全转化为NH4NO3.
解答 解:由流程可知,吸收池I中发生SO2+OH-=HSO3-、CO2+OH-=HCO3-,NO不反应,吸收池Ⅲ中,酸性条件下NO转化为NO2-,发生NO+H2O+Ce4+=Ce3++NO2-+2H+,吸收池Ⅳ中NaHSO3溶液中HSO3-的电离大于水解,HSO3-?SO32-+H+,溶液显示酸性,加入CaCl2溶液后,Ca2++SO32-=CaSO3↓使电离平衡右移,电解池Ⅴ可使Ce4+再生,Ce失去电子在阳极得到,阴极上发生2HSO3-+4H++4e-=S2O32-+3H2O,氧化池Ⅵ中得到粗产品NH4NO3,
(1)由上述分析可知,可循环利用,且流程中CO2回收应用,故答案为:Ce4+、CO2;
(2)乙醇胺(HOCH2CH2NH2),其水溶液具有弱碱性,显碱性的原因:HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-,乙醇胺吸收CO2的化学方程式为HOCH2CH2NH2+H2O+CO2=HOCH2CH2NH4HCO3,
故答案为:HOCH2CH2NH2+H2O+CO2=HOCH2CH2NH4HCO3;
(3)吸收池Ⅲ中,酸性条件下NO转化为NO2-的离子方程式为NO+H2O+Ce4+=Ce3++NO2-+2H+,故答案为:NO+H2O+Ce4+=Ce3++NO2-+2H+;
(4)NaHSO3溶液中HSO3-的电离大于水解,HSO3-?SO32-+H+,溶液显示酸性,加入CaCl2溶液后,Ca2++SO32-=CaSO3↓使电离平衡右移,
故答案为:HSO3-在溶液中存在电离平衡:HSO3-?SO32-+H+,加CaCl2溶液后,Ca2++SO32-=CaSO3↓使电离平衡右移,c(H+)增大;
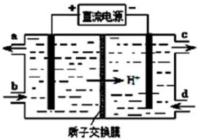
(5)在电解池中,阳极上是Ce3+失电子成为Ce4+的过程,所以生成Ce4+从电解槽的阳极上极a极流出,电解池的阴极发生得电子的还原反应,电极反应式为2HSO3-+4H++4e-=S2O32-+3H2O,
故答案为:a;2HSO3-+4H++4e-=S2O32-+3H2O;
(6)在氧化池Ⅵ中得到NH4NO3溶液,从NH4NO3溶液中得到硝酸铵可以通过蒸发浓缩,冷却结晶、过滤、洗涤等操作获得,
故答案为:蒸发浓缩、冷却结晶.
点评 本题考查混合物分离提纯,为高频考点,把握流程中的反应及混合物分离方法选择为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度较大.


科目:高中化学 来源: 题型:解答题

 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | Z | |
| A. | FeCl2溶液 | FeCl3 | KSCN溶液 |
| B. | Al粉 | Fe粉 | NaOH溶液 |
| C. | Fe2(SO4)3溶液 | FeSO4 | Cl2 |
| D. | FeCl2溶液 | CuCl2 | Fe粉 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2溶于水且显酸性 | |
| B. | 点燃是H2和Cl2化合的惟一条件 | |
| C. | SiO2是酸性氧化物,它不溶于任何酸 | |
| D. | 液氯和氯水不是同一物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 澄清透明的无色溶液:K+、NH4+、MnO4-、HCO3- | |
| B. | 0.10 mol•L-1 KI溶液:Al3+、Fe3+、Cl-、SO42- | |
| C. | 滴入甲基橙变红色的溶液:Na+、Ca2+、NO3-、Cl- | |
| D. | c(H+)=1×10-12 mol•L-1的溶液:Mg2+、Cu2+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-725.8 kJ/mol | |
| B. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=-1451.6 kJ/mol | |
| C. | CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=+725.8 kJ/mol | |
| D. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1451.6 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X与Y形成原子个数比1:1的化合物只有2种 | |
| B. | Y、W的氧化物均为酸性氧化物 | |
| C. | 最高价氧化物对应水化物的酸性:Y<W | |
| D. | X与Z形成的化合物中,各原子均满足8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com