
| A£® | Äę·“Ó¦ĖŁĀŹŅ»¶ØŌö“ó | B£® | Ę½ŗāŅ»¶ØĻņÕż·“Ó¦·½Ļņ½ųŠŠ | ||
| C£® | ·“Ó¦ĪļµÄ×Ŗ»ÆĀŹŅ»¶ØŌö“ó | D£® | øĆ·“Ó¦µÄĢõ¼žŅ»¶Ø·¢Éś±ä»Æ |
·ÖĪö ijæÉÄę·“Ó¦µ±Õż·“Ó¦ĖŁĀŹŌö“óŹ±£¬Äę·“Ó¦ĖŁĀŹæÉÄÜŌö“óŅ²æÉÄܲ»±ä£¬Čē¹ūŹĒĶعżøıäŃ¹Ē攢ĪĀ¶Č”¢“߻ƼĮŹ±£¬Äę·“Ó¦ĖŁĀŹŌö“ó£¬Čē¹ūøıäµÄŹĒ·“Ó¦ĪļÅØ¶Č£¬ŌņÄę·“Ó¦ĖŁĀŹ²»±ä£¬¾Ż“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗA£®Ä³æÉÄę·“Ó¦µ±Õż·“Ó¦ĖŁĀŹŌö“óŹ±£¬Čē¹ūøıäµÄŹĒ·“Ó¦ĪļÅØ¶Č£¬Éś³ÉĪļÅØ¶Č²»±ä£¬ŌņÄę·“Ó¦ĖŁĀŹ²»±ä£¬¹ŹA“ķĪó£»
B£®Čē¹ūøıäĢõ¼žŹ±ÄÜĶ¬µČ³Ģ¶ČµÄŌö“óÕżÄę·“Ó¦ĖŁĀŹ£¬ŌņĘ½ŗā²»ŅĘ¶Æ£¬¹ŹB“ķĪó£»
C£®Čē¹ūŌö“ó·“Ó¦ĪļÅØ¶Č¶ųŌö“óÕż·“Ó¦ĖŁĀŹ£¬ŅņĪŖ¼ÓČė·“Ó¦ĪļµÄĮæŌ¶Ō¶“óÓŚĘä×Ŗ»ÆŌö¼ÓµÄĮ棬ĖłŅŌ·“Ó¦Īļ×Ŗ»ÆĀŹæÉÄܽµµĶ£¬¹ŹC“ķĪó£»
D£®æÉÄę·“Ó¦Ę½ŗāדĢ¬ŹĒ¶ÆĢ¬Ę½ŗā£¬Ģõ¼žøı䣬·“Ó¦ĖŁĀŹøı䣬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²é»Æѧ·“Ó¦ĖŁĀŹµÄÓ°ĻģŅņĖŲ£¬ĪŖøßĘµæ¼µć£¬Ć÷Č··“Ó¦ĖŁĀŹøıäŌĄķŹĒ½ā±¾Ģā¹Ų¼ü£¬Ķ¬Ź±æ¼²éѧɜ·¢É¢Ė¼Ī¬ÄÜĮ¦£¬×¢Ņā·“Ó¦ĖŁĀŹøıäĘ½ŗā²»Ņ»¶ØŅĘ¶Æ£¬ŅדķŃ”ĻīŹĒB£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1mol SiO2ÖŠŗ¬ÓŠNAøöSiO2·Ö×Ó | |
| B£® | 1mol CuÓė×ćĮæµÄĻ”HNO3·“Ó¦£¬×ŖŅĘ2 NAøöµē×Ó | |
| C£® | 1 LO.1mol•L-1Na2CO3 ČÜŅŗÖŠŗ¬ÓŠ 0.1NA øöCO${\;}_{3}^{2-}$ | |
| D£® | 1mol±½ŅŅĻ©ÖŠŗ¬ÓŠµÄĢ¼Ģ¼Ė«¼üŹżĪŖ4Na |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻČÅäÖĘ0.10 mol/L CH3COOHČÜŅŗ£¬ŌŁ²āČÜŅŗµÄpH£¬ČōpH“óÓŚ1£¬ŌņæÉÖ¤Ć÷“×ĖįĪŖČõµē½āÖŹ | |
| B£® | ĻČÅäÖĘ0.01 mol/LŗĶ0.10 mol/LµÄCH3COOH£¬ŌŁ·Ö±šÓĆpH¼Ę²āĖüĆĒµÄpH£¬ČōĮ½ÕßµÄpHĻą²īŠ”ÓŚ1øöµ„Ī»£¬ŌņæÉÖ¤Ć÷“×ĖįŹĒČõµē½āÖŹ | |
| C£® | Č”µČĢå»ż”¢µČpHµÄCH3COOHµÄČÜŅŗŗĶŃĪĖį·Ö±šÓė×ćĮæŠæ·“Ó¦£¬²āµĆ·“Ó¦¹ż³ĢÖŠ“×Ėį²śÉśH2ĖŁĀŹ½ĻĀżĒŅ×īÖÕ²śÉśH2½Ļ¶ą£¬ŌņæÉÖ¤Ć÷“×ĖįĪŖČõµē½āÖŹ | |
| D£® | ÅäÖĘŅ»¶ØĮæµÄCH3COONaČÜŅŗ£¬²āĘäpH£¬Čō³£ĪĀĻĀpH“óÓŚ7£¬ŌņæÉÖ¤Ć÷“×ĖįŹĒČõµē½āÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
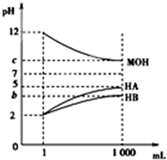 ŹŅĪĀĻĀ£¬½«pH=2µÄĮ½ÖÖĖįČÜŅŗHA”¢HBŗĶpH=12µÄ¼īČÜŅŗMOHø÷1mL£¬·Ö±š¼ÓĖ®Ļ”ŹĶµ½1 000mL£¬ĘäpHµÄ±ä»ÆÓėČÜŅŗĢå»żµÄ¹ŲĻµČēĶ¼£¬ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©
ŹŅĪĀĻĀ£¬½«pH=2µÄĮ½ÖÖĖįČÜŅŗHA”¢HBŗĶpH=12µÄ¼īČÜŅŗMOHø÷1mL£¬·Ö±š¼ÓĖ®Ļ”ŹĶµ½1 000mL£¬ĘäpHµÄ±ä»ÆÓėČÜŅŗĢå»żµÄ¹ŲĻµČēĶ¼£¬ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©| A£® | HAĪŖĒæĖį£¬HBĪŖČõĖį | |
| B£® | Čōb+c=14£¬ŌņMOHĪŖČõ¼ī | |
| C£® | Čōc=9£¬ŌņĻ”ŹĶŗóµÄČżÖÖČÜŅŗÖŠ£¬ÓÉĖ®µēĄėµÄĒāĄė×ÓµÄÅØ¶ČµÄ“óŠ”Ė³ŠņĪŖHA£¾MOH£¾HB | |
| D£® | Čōc=9£¬½«Ļ”ŹĶŗóµÄHAČÜŅŗŗĶMOHČÜŅŗČ”µČĢå»ż»ģŗĻ£¬ŌņĖłµĆČÜŅŗÖŠc£ØA-£©=c£ØM+£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
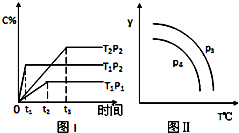 ŌŚÄ³ČŻ»żŅ»¶ØµÄĆܱÕČŻĘ÷ÖŠ£¬ÓŠĻĀĮŠæÉÄę·“Ó¦xA£Øg£©+B£Øg£©?2C£Øg£©£¬·“Ó¦ĒśĻߣØT±ķŹ¾ĪĀ¶Č£¬P±ķŹ¾Ń¹Ē棬C% ±ķŹ¾CµÄĢå»ż·ÖŹż£©ČēĶ¼ĖłŹ¾£¬ŹŌÅŠ¶Ļ¶ŌĶ¼µÄĖµ·ØÖŠŅ»¶ØÕżČ·µÄŹĒ£Ø””””£©
ŌŚÄ³ČŻ»żŅ»¶ØµÄĆܱÕČŻĘ÷ÖŠ£¬ÓŠĻĀĮŠæÉÄę·“Ó¦xA£Øg£©+B£Øg£©?2C£Øg£©£¬·“Ó¦ĒśĻߣØT±ķŹ¾ĪĀ¶Č£¬P±ķŹ¾Ń¹Ē棬C% ±ķŹ¾CµÄĢå»ż·ÖŹż£©ČēĶ¼ĖłŹ¾£¬ŹŌÅŠ¶Ļ¶ŌĶ¼µÄĖµ·ØÖŠŅ»¶ØÕżČ·µÄŹĒ£Ø””””£©| A£® | øĆ·“Ó¦ŹĒĪüČČ·“Ó¦ | |
| B£® | x=2 | |
| C£® | P3£¼P4£¬yÖįæɱķŹ¾»ģŗĻĘųĢåµÄĻą¶Ō·Ö×ÓÖŹĮæ | |
| D£® | P3£¾P4£¬yÖįæɱķŹ¾CĪļÖŹŌŚĘ½ŗāĢå»żÖŠµÄ°Ł·Öŗ¬Įæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
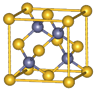 ¢ń£®øõĪ»ÓŚµŚĖÄÖÜĘŚ¢öB×壬Ö÷ŅŖ»ÆŗĻ¼Ū+2£¬+3£¬+6£¬µ„ÖŹÓ²¶Č“ó£¬ÄĶøÆŹ“£¬ŹĒÖŲŅŖµÄŗĻ½š²ÄĮĻ£®
¢ń£®øõĪ»ÓŚµŚĖÄÖÜĘŚ¢öB×壬Ö÷ŅŖ»ÆŗĻ¼Ū+2£¬+3£¬+6£¬µ„ÖŹÓ²¶Č“ó£¬ÄĶøÆŹ“£¬ŹĒÖŲŅŖµÄŗĻ½š²ÄĮĻ£®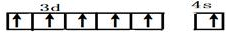 £¬CrO2Cl2³£ĪĀĻĀĪŖÉīŗģÉ«ŅŗĢ壬ÄÜÓėCCl4”¢CS2µČ»„ČÜ£¬¾Ż“ĖæÉÅŠ¶ĻCrO2Cl2ŹĒ·Ē¼«ŠŌ£ØĢī”°¼«ŠŌ”±»ņ”°·Ē¼«ŠŌ”±£©·Ö×Ó£®
£¬CrO2Cl2³£ĪĀĻĀĪŖÉīŗģÉ«ŅŗĢ壬ÄÜÓėCCl4”¢CS2µČ»„ČÜ£¬¾Ż“ĖæÉÅŠ¶ĻCrO2Cl2ŹĒ·Ē¼«ŠŌ£ØĢī”°¼«ŠŌ”±»ņ”°·Ē¼«ŠŌ”±£©·Ö×Ó£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
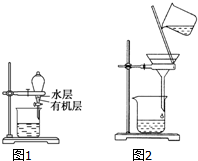
| A£® | ·ÖĄėŅŅ“¼ŗĶŅŅĖįŅŅõ„µÄ»ģŗĻĪļ£¬ĖłÓĆ²£Į§ŅĒĘ÷ĪŖ·ÖŅŗĀ©¶·”¢ÉÕ± | |
| B£® | ÓĆČēĶ¼1ĖłŹ¾×°ÖĆ·ÖĄėCCl4ŻĶČ”µāĖ®ŗóŅŃ·Ö²ćµÄÓŠ»ś²ćŗĶĖ®²ć | |
| C£® | ÓƱ½ŻĶČ”äåĖ®ÖŠµÄäåŹ±£¬½«äåµÄ±½ČÜŅŗ“Ó·ÖŅŗĀ©¶·ĻĀæŚ·Å³ö | |
| D£® | ÓĆČēĶ¼2ĖłŹ¾×°ÖĆ³żČ„ŅŅ“¼ÖŠµÄ±½·Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ĖįŠŌŠæĆĢøɵē³ŲŗĶ¼īŠŌŠæĆĢøɵē³Ų | B£® | Ē¦Šīµē³Ų | ||
| C£® | ĒāĘųČ¼ĮĻµē³ŲŗĶ¼×ĶéČ¼ĮĻµē³Ų | D£® | ÄųļÓµē³ŲŗĶļ®µē³Ų |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com