
| A、只有①④⑦ | B、只有②⑥ |
| C、只有②⑤⑥ | D、只有③⑦ |


科目:高中化学 来源: 题型:
| 高温 |
| m |
| n |
| m |
| n |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、增加C的质量 |
| B、保持体积不变,充入氦气使体系压强增大 |
| C、加入催化剂 |
| D、保持压强不变,充入氦气使容器体积增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2和H3属于同位素 |
| B、O2+中不含化学键 |
| C、C60中含有共价键 |
| D、N5+中含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若保持恒容,充入C气体后混合气体颜色加深,则说明B是有颜色的气体 |
| B、若升高温度,发现C的物质的量减少,则说明正反应为放热反应 |
| C、若压缩容器,平衡不移动,则说明B和D一定都是气体 |
| D、保持恒容,到达平衡后继续充入A会使B的转化率增大,A的转化率减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
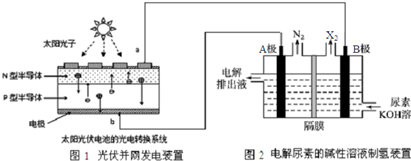
| A、图1中N型半导体为正极,P型半导体为负极 |
| B、图2溶液中电子流向:从B极流向A极 |
| C、X2为氧气 |
| D、工作时,A极的电极反应式为CO(NH2)2+8OH--6e-═CO32-+N2↑+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:2 | B、1:3 |
| C、2:3 | D、3:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com