
����Ŀ����һ���Ȼ�������Ʒ�����л���������AlCl3��FeCl3�����ʣ�ijС��Ϊ���ᴿ�Ȼ�����������������ʵ�顣

��1������ii��Ŀ����____________�������ӷ���ʽΪ____________��
��2����ҺC����������____________����Ӧiii�����ӷ�Ӧ����ʽΪ____________��
��3����������ʵ�飬��������˵������������_______
����ҺB�к��н�������ֻ������
����ҺC�������ֽ���������
������D���ȿɷֽ�
��4��������Ʒ���������жϼ���1mol/L NaOH��Һ�����������Ϊ__________��
�� 40mL �� 400mL �� 4L
���𰸡� ����Fe2+ΪFe3+ 2Fe2+ +Cl2=2Fe3+ +2Cl- AlO2-��OH-��Cl- Al3++4OH-=AlO2-+2H2O ��Fe3++3OH-=Fe(OH)3�� �٢� ��
������������i��Ʒ��ˮ�γ���ҺA�к���FeCl2��AlCl3��FeCl3������iiͨ��������Fe2+ ����ΪFe3+����ҺBΪAlCl3��FeCl3������iii�ӹ�����NaOH��Һ��Al3�����AlO2��������ҺC�У�����DΪFe(OH)3���ټ�������FeCl3��������ԭ��FeCl2��
��1������ii��Ŀ��������Fe2+ΪFe3+�������ӷ���ʽΪ2Fe2+ +Cl2=2Fe3+ +2Cl-����2��AlCl3��FeCl3�����Һ�мӹ�����NaOH��Һ��Al3�����AlO2����������OH-��δ��Ӧ��Cl-����ҺC���������� AlO2-��OH-��Cl-����Ӧiii�����ӷ�Ӧ����ʽΪAl3++4OH-=AlO2-+2H2O ��Fe3++3OH-=Fe(OH)3�� ����3������ҺB�к��н��������У�Fe3+��Al3+�Լ�Al3+ˮ�����ɵ�Al��OH��4�����ʴ���������ҺC����һ�ֽ���������Na�����ʴ���������DΪFe(OH)3���ȿɷֽ⣬����ȷ����ѡ�٢ڣ���4��������Ʒ��������13.0gFeCl2�����ʵ���ԼΪ��13.0g/127g��mol��1=0.1mol������������������0.1molFeCl3������1mol/L NaOH��Һ�����������ֵ����300mL,��ѡ�ڡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ѧ��ѧ�г����ڻ����ķ�����ᴿ��װ����
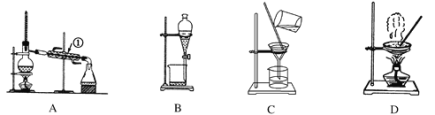
��������װ�ã���������ʵ�鷽���Ӻ��������������ȡ���п��������Ե���Ȼ�������֪�ױ��ͼ״���Ϊ�л��ܼ����л������ܻ��ܣ�

��1��װ��A�������ٵ�������________��ʹ��װ��A�IJ�����_____���a������b������c����d������ͬ����
��2��ʹ��װ��B�IJ�����______��Ϊʹ����Һ��˳�����£������¶˻����⣬��Ӧ���еľ��������___________________��
��3��ʹ��װ��C�IJ�����_______�������ó���������ˮ����Ҫϴ�ӣ���ϴ�ӵľ��������________________________________________________________________________________��
��4��ʹ��װ��D�IJ�����_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ�鼰����ó��Ľ�����ȷ����
ʵ�� | ���� | ���� | |
A | SO2��H2S������ | ��������ɫ���� | ������:SO2>S |
B | ��ʢ��FeSO4��Һ���Թ��е�����ˮ��Ȼ�����KSCN��Һ | ����KSCN����Һ��Ϊ��ɫ | ԭFeSO4��Һ�ѱ�������O2�������� |
C | �Թ���ʢ��Cu(NO3)2��Һ���ײ�������ͭ�������м���ϡ���� | ͭ�����ܽ� | ͭ����ϡ���ᷴӦ |
D | ��2֧ʢ��2mL��ͬŨ�ȵ�NaOH��Һ���Թ��зֱ����2����ͬŨ�ȵ�AlCl3��MgCl2��Һ�������� | ǰ�������������а�ɫ���� | Ksp[Al(OH)3]>Ksp[Mg(OH)2] |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Na2O2���������������еĹ�������Ӧ����DZͧ�С��䷴Ӧԭ����2Na2O2+2CO2=2Na2CO3+O2���÷�Ӧ�У���ԭ����________����������________������ÿ����22.4L CO2���壨��״�������ܹ�����_________L��������״������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ�������ʵ�鷽�����Է���NaCl��BaCl2���ֹ�������ش��������⣺

��ѡ�Լ���Na 2CO3��Һ��Na2SO4��Һ��K2CO3��Һ��K2SO4��Һ������
��1����������������______________��
��2���Լ�a��________(�ѧʽ����ͬ)���Լ�b��____________������B��________��
��3�������Լ�a�������Ļ�ѧ��Ӧ����ʽΪ_______________________________________��
��4������ϴ�ӵIJ�������____________________________________________________________��
��5���÷����ܷ�ﵽʵ��Ŀ��?___________�������ܣ�Ӧ��θĽ�(���ܣ����ʲ��ûش�)________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��SCR��������Ч���Ͳ��ͷ�����β����NOx���ŷš�SCR��ѡ���Դ���ԭ������ԭ����ͼ��ʾ��
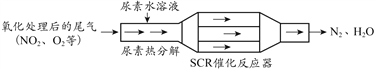
��1������β��ֱ���ŷŻ����_______
a. ���������� b. ���������� c. ������ն�
��2������[CO(NH2)2]ˮ��Һ�ȷֽ�ΪNH3��CO2����Ӧ����NH3���Ի�ԭNO2����ת���к�����Ϊ�����ʵ����ã���֪�μӷ�Ӧ�İ�����NO2�������Ϊ��:�����䷴Ӧ����ʽΪ_________��
��3������Ԫ���غ㣬���մ����������N2��H2O������_______��
��4����ͨ��β���к�67.2L NO2����״���������백����ȫ��Ӧת�Ƶ�����Ϊ_____mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����![]() ��ʾ����٤��������ֵ������˵������ȷ����
��ʾ����٤��������ֵ������˵������ȷ����![]() ����
����![]()
A. ![]() �����е�ԭ����Ϊ
�����е�ԭ����Ϊ![]()
B. ��״���£�![]() ˮ�к��е�ˮ������Ϊ
ˮ�к��е�ˮ������Ϊ![]()
C. ��״���£�![]() �����ķ�����Ϊ
�����ķ�����Ϊ![]()
D. ![]() ��Һ��������
��Һ��������![]() Ϊ
Ϊ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����������е�������������
A. ��ơ��ƿ��ƿ�ǣ�����������ð������������������������ԭ������
B. ���Ṥҵ��SO2ת��ΪSO3ʱ���ó�ѹ������Ϊ����ѹǿ�������SO2��ת����
C. ��ҵ�Ϻϳɰ�����500�����ҵ��¶ȣ���ԭ�����ʵ��ӿ�NH3�ĺϳ����ʣ�������500������ʱ��������
D. �ȼҵ�������ӽ���Ĥ���۵��ʱ����������ע�뾭�����Ƶ�NaCl��Һ����������ע��ϡ����������Һ����ȥ����ˮ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij�л��������ֻ����C��N��H����Ԫ�أ���n(C)��n(N)�ֱ��ʾC��N��ԭ����Ŀ����Hԭ�������Ϊ �� ��
A. 2n(C)+2+n(N) B. 2n(C)+2+2n(N)
C. 2n(C)+1+2n(N) D. 3n(C)+2n(N)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com