
| A. | 上述反应是放热反应 | B. | 上述反应是吸热反应 | ||
| C. | a+b>c | D. | a+b<c |
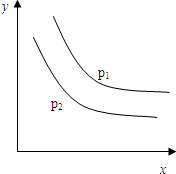
分析 图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数,则相同压强下,温度越高,G的体积分数越小;相同温度时,压强越大,G的体积分数越大,结合化学平衡移动原理分析升温平衡向吸热反应方向进行,增大压强平衡向气体体积减小的方向进行,以此来解答.
解答 解:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数,则相同压强下,温度越高,G的体积分数越小,所以该反应为吸热反应;
相同温度时,压强越大,G的体积分数越大,则增大压强,平衡逆向移动,因L为固体,所以b<c,
故选B.
点评 本题考查化学平衡的影响因素,把握温度、压强对平衡的影响及图象的分析为解答的关键,注意图象中定一议二与平衡移动相结合,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | SO2有漂白性,所以能使滴有酚酞的NaOH溶液褪色 | |
| B. | SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,其原理相同 | |
| C. | 能使品红溶液褪色的不一定是SO2 | |
| D. | SO2和Cl2都能漂白,若将两种气体同时通入,漂白效果会更好 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
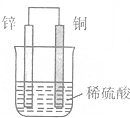
| A. | 锌片上有H2逸出 | B. | 溶液中c(H+)逐渐减小 | ||
| C. | 正极反应式:2H++2e-═H2↑ | D. | 负极反应式:Zn-2e-═Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
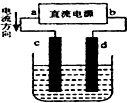
| A. | c、d电极上都有气体产生 | B. | d为阴极、c为阳极 | ||
| C. | d极附近溶液PH值升高 | D. | 电解过程中,氯离子浓度减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在相同条件下的溶解度:NaHCO3>Na2CO3 | |
| B. | 还原性:I->Br->Cl->F- | |
| C. | 氧化性:F2>Cl2>Br2>I2 | |
| D. | 碳酸氢钠溶液与稀盐酸互滴时两种操作现象相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
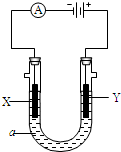 电解原理在化学工业中有广泛应用,如图为工业制氯气的装置原理.U型管中装有电解液a;X、Y是两根电极棒,通过导线与直流电源相连,实验开始时,同时在两边各滴入几滴酚酞试液.请回答以下问题:
电解原理在化学工业中有广泛应用,如图为工业制氯气的装置原理.U型管中装有电解液a;X、Y是两根电极棒,通过导线与直流电源相连,实验开始时,同时在两边各滴入几滴酚酞试液.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性 | |
| B. | 向稀硝酸中加入铁粉完全反应,所得溶液一定只含一种溶质 | |
| C. | 将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 | |
| D. | 在含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热,除去过量的Cl2,即可得到较纯净FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
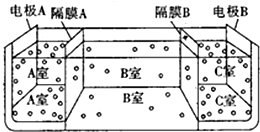
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
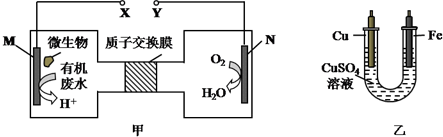
| A. | H十透过质子交换膜由右向左移动 | |
| B. | 铜电极应与X相连接 | |
| C. | M电极反应式:H2NCONH2+H2O-6e-═CO2↑+N2↑+6H+ | |
| D. | 当N电极消耗0.25mol气体时,则铁电极增重16g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com