
【题目】最近,科学家合成了含有N![]() 的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈“V”形,如图所示,以下有关该物质的说法中正确的是( )
的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈“V”形,如图所示,以下有关该物质的说法中正确的是( )

A.每个N![]() 中含有35个质子和36个电子
中含有35个质子和36个电子
B.该离子中有非极性键和配位键
C.该离子中含有2个π键
D.与PCl![]() 互为等电子体
互为等电子体
 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
【题目】下列说法或表示方法中正确的是( )
A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B.由C(金刚石)=C(石墨)![]() <0,可知,金刚石比石墨稳定
<0,可知,金刚石比石墨稳定
C.在101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l) ![]() = -571.6kJ/mol
= -571.6kJ/mol
D.在稀溶液中,若将含0.5mol H2SO4的浓溶液与含1mol NaOH的溶液混合,放出的热量大于57.3kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖酸亚铁((C6H11O7)2Fe)是常用的补铁剂,易溶于水,几乎不溶于乙醇。用下图装置制备FeCO3,并利用FeCO3与葡萄糖酸反应可得葡萄糖酸亚铁。回答下列问题:

(1)a的名称为_________。
(2)打开a中K1、K3,关闭K2,一段时间后,关闭K3,打开K2。在_________(填仪器标号)中制得碳酸亚铁。实验过程中产生的H2作用有_________、____________。(写2条)
(3)将制得的碳酸亚铁浊液过滤、洗涤。如过滤时间过长会发现产品部分变为红褐色。用化学方程式说明原因____________。
(4)将葡萄糖酸与碳酸亚铁混合,加入乙醇、过滤、洗涤、干燥。加入乙醇的目的是_________________。
(5)用 NaHCO3溶液代替Na2CO3溶液制备碳酸亚铁,同时有气体产生,离子方程式为______________,此法产品纯度更高,原因是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铬矿石(主要成分为Cr2O3,还有Al2O3、SiO2等杂质)为原料制取红矾钠 (Na2Cr2O7·2H2O)的流程如图所示。
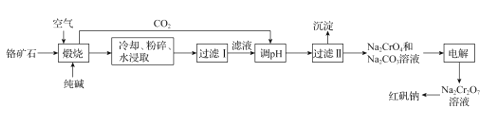
已知:I.Cr2O3在碱性条件下易被氧化;
II.高温条件下,Al2O3与Na2CO3发生的反应为:Al2O3 +Na2CO3=2NaAlO2 +CO2↑;
III.2CrO42-+2H+![]() Cr2O72- +H2O K=1.0×1012
Cr2O72- +H2O K=1.0×1012
(1)“煅烧”时,Cr2O3参加反应的化学方程式为_____。若“煅烧”操作最适宜的温度是800~900℃,则在实验室中进行此项操作时,应选择_____坩埚(填字母)。
a.陶瓷 b.玻璃 c.石英 d.铁
(2)流程中可循环利用的物质除CO2外还有_____(填化学式)。
(3)“过滤II”所得沉淀主要有______(填化学式)。
(4)由Na2Cr2O7溶液制备红矾钠的具体实验操作有_____,经洗涤、干燥得到红矾钠样品。
(5)“电解”时,利用以下装置将Na2CrO4溶液转化为Na2Cr2O7溶液,当a、b均为石墨电极时,a电极的电极反应式为____。若初始加入电解池中的c (Na2CrO4)=1.0mol·L-l,随着“电解”的进行,当溶液pH=6时,Na2CrO4的转化率为______(忽略电解过程中溶液体积变化)。
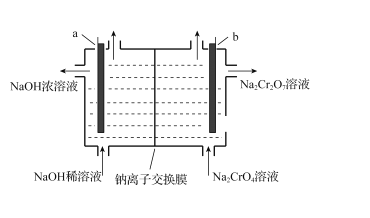
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语或描述中,正确的是
A.离子结构示意图  既可以表示35Cl-,也可以表示37Cl-
既可以表示35Cl-,也可以表示37Cl-
B.SO3的水溶液能导电,说明SO3是电解质
C.NaHSO3在水中的电离方程式:NaHSO3=Na++H++SO32-
D.同素异形体间的转化和同位素间的转化都是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的认识不正确的是( )
A.乙醇与乙酸在一定条件下可发生酯化反应
B.四氯化碳为有机非极性溶剂
C.在水溶液里,乙酸分子中的—CH3可以电离出H+
D.在浓硫酸存在下,苯与浓硝酸共热生成硝基苯的反应属于取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下对甲基苯甲醚为无色液体,具有紫罗兰的香气,可由对甲基苯酚与甲醇在浓硫酸催化作用下制取,反应装置(部分夹持装置已略去)如图所示:

制备反应为![]() +CH3OH
+CH3OH![]()
![]() +H2O。可能用到的数据如下:
+H2O。可能用到的数据如下:
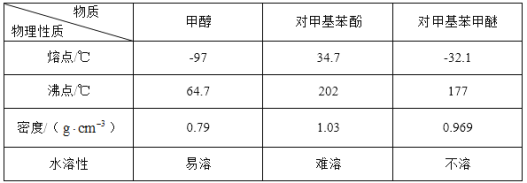
Ⅰ.合成反应:在图1的烧瓶中先加入几片碎瓷片,再依次加入10.8g对甲基苯酚、10mL甲醇,最后加入2mL浓硫酸,控制反应温度为60℃(水浴加热)进行反应。
Ⅱ.产物提纯:①将反应混合液冷却后加入足量饱和碳酸钠溶液,充分反应后转移至分液漏斗中,静置分液;②将有机层转移至图2烧瓶中,加热,控制温度为100℃进行蒸馏,待蒸馏结束后,向烧瓶内剩余液体中加入足量无水氯化钙,然后趁热过滤,并将所得液体再次进行蒸馏,收集177℃左右馏分,蒸馏结束后,称量所得馏分为7.32g。
回答下列问题:
(1)仪器A的名称为__。
(2)向图1的烧瓶中加入碎瓷片的目的是__;采用水浴加热的目的是__。
(3)产物提纯时,向反应混合液中加入足量饱和碳酸钠溶液的作用是__;产物提纯时,先控制温度为100℃进行蒸馏的目的是__。
(4)加入足量无水氯化钙的目的是__。
(5)收集到的177℃左右的馏分主要是__(填名称)。
(6)对甲基苯甲醚的产率为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com