
| A�� | Q1��Q2��Q2=2Q3 | B�� | Q1=Q2=Q3 | C�� | Q1��Q2��Q3=$\frac{{Q}_{1}}{2}$ | D�� | ���Ƚ� |
���� ������ȫȼ������Һ̬ˮ��������̬ˮ�ų��������࣬��ΪҺ̬ˮ��Ϊ��̬ˮ��Ҫ���ȣ�ȼ��2mol������ȼ��1 mol����������̬ˮ�ų���������2�����Դ˽����⣮
��� �⣺��ΪҺ̬ˮ��Ϊ��̬ˮ��Ҫ���ȣ���������ȫȼ������Һ̬ˮ��������̬ˮ�ų��������࣬��1���루2���Ƚϣ�Q2��Q1��
ȼ��2 mol������ȼ��1 mol����������̬ˮ�ų���������2������1���루3���Ƚϣ�2Q3=Q1��
��ѡC��
���� ���⿼�鷴Ӧ�ȴ�С�ıȽϣ���Ŀ�ѶȲ�����ע����ձȽϷ�Ӧ�ȴ�С�ķ�����


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
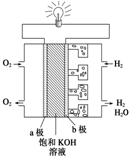 I����Դ�������������ᷢչ�Ļ��������������������Դ��̫���ܣ�����Ȼ������һ��Դ��ɹ�����ֲ��Ĺ�����ã����������ǿ����������ɫ��Դ����֪��������ֵ��143kJ•g-1����ֵָ������һ�������µ�λ������������ȫȼ�����ų�������������ת��ΪҺ̬ˮ������д������ȼ�յ��Ȼ�ѧ����ʽH2��g��+$\frac{1}{2}$O2��g��=H2O��1������H=-286kJ•mol-1��2H2��g��+O2��g��=2H2O��l����H=-572KJ•mol-1��
I����Դ�������������ᷢչ�Ļ��������������������Դ��̫���ܣ�����Ȼ������һ��Դ��ɹ�����ֲ��Ĺ�����ã����������ǿ����������ɫ��Դ����֪��������ֵ��143kJ•g-1����ֵָ������һ�������µ�λ������������ȫȼ�����ų�������������ת��ΪҺ̬ˮ������д������ȼ�յ��Ȼ�ѧ����ʽH2��g��+$\frac{1}{2}$O2��g��=H2O��1������H=-286kJ•mol-1��2H2��g��+O2��g��=2H2O��l����H=-572KJ•mol-1���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ͬ��Ŀ��ԭ�� | B�� | ��ռ22.4 L | ||
| C�� | ������ͬ��Ŀ�ķ��� | D�� | ������ͬĦ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������������ | |
| B�� | ��ϵ�д��������������ij����ܽ�ƽ�� | |
| C�� | ��Һ�в��ٴ���Fe3+ | |
| D�� | �����������ᣬ����Һ��Fe3+Ũ�Ȼ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.5 mol | B�� | 0.6 mol | C�� | 0.7 mol | D�� | 0.8 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
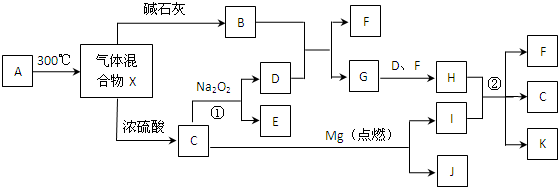
 ����A��B��C���ֶ�����Ԫ�أ�ԭ���������ε�����A��C��������֮��Ϊ27������������֮��Ϊ5��0.9g����B���������ᷴӦ���ռ�������1.12L����״��������ش��������⣺
����A��B��C���ֶ�����Ԫ�أ�ԭ���������ε�����A��C��������֮��Ϊ27������������֮��Ϊ5��0.9g����B���������ᷴӦ���ռ�������1.12L����״��������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
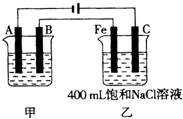 ������ϵͳ��������д�����и���������
������ϵͳ��������д�����и���������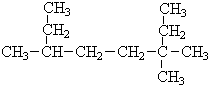 ��3��3��6-��������
��3��3��6-���������鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com